��Ŀ����
17����ͼ��ʵ�����Ʊ�����������һϵ�����ʵ���װ�ã��г��豸���ԣ���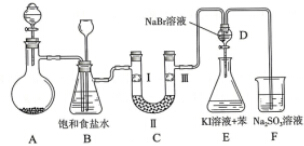
��1���Ʊ�����ѡ�õ�ҩƷΪ��Ư�������Ũ���ᣬƯ������Ч�ɷ���Ca��ClO��2������Ũ�����ڳ����¼��ɷ�Ӧ����صĻ�ѧ��Ӧ����ʽΪCa��ClO��2+4HCl��Ũ���TCaCl2+2Cl2��+2H2O��
��2��װ��B�б���ʳ��ˮ�������dz�ȥCl2��HCl��ͬʱװ��B���ǰ�ȫƿ�����ʵ�����ʱC���Ƿ������������C���������ˣ���B�е�����B�г���©����Һ���������γ�һ��ˮ������ƿ��Һ���½���
��3��װ��C��ʵ��Ŀ������֤�����Ƿ����Ư���ԣ�Ϊ��C�Т����η���d��
| a | b | c | d | |
| �� | �������ɫ���� | �������ɫ���� | ʪ�����ɫ���� | ʪ�����ɫ���� |
| �� | ��ʯ�� | �轺 | Ũ���� | ��ˮ�Ȼ��� |
| �� | ʪ�����ɫ���� | ʪ�����ɫ���� | �������ɫ���� | �������ɫ���� |
��5����������װ��D��������Һ����װ��E�У����۲쵽��������E����Һ��Ϊ���㣬�ϲ㣨���㣩Ϊ�Ϻ�ɫ��
��6�����������װ��F�пɸ���������NaHSO3��Һ�������ȣ���д����Ӧ�����ӷ�Ӧ����ʽ��HSO3-+Cl2+H2O=SO42-+2Cl-+3H+��4HSO3-+Cl2=SO42-+2Cl-+3SO2��+2H2O���жϸ���NaHSO3��Һ�Ƿ���з���ǡ�����
���� ��1��Ư������Ч�ɷ��Ǵ�����ƣ����������Ũ���ᷴӦ�����Ȼ��ơ�������ˮ��
��2�������ӷ�����Ӧ��ȡ�������к����Ȼ��⣬�Ȼ���������ˮ�������ڱ���ʳ��ˮ���ܽ�Ȳ���
װ��B���ǰ�ȫƿ�����ʵ�����ʱC���Ƿ�����������������ʱB�еģ�ѹǿ����
��3��Ϊ����֤�����Ƿ����Ư���ԣ�Ҫ��֤����������Ư���ԣ�ʪ�����ɫ�����У�������ˮ��Ӧ���ɴ��������Ư���ԣ�
��4��ͨ���û���Ӧ����֤�������塢���������ǿ�����Ƚ��ȡ��塢��ķǽ����ԣ�
��5����������װ��D��������Һ����װ��E�У����ɵ��嵥�ʺ͵⻯�ط�Ӧ���ɵⵥ�ʣ��ⵥ���ܽ��ڱ��У��ֲ㣬�������ϲ㣻
��6����������ǿ�����ԣ�����Һ�н�SO32-����SO42-ͬʱ����Cl-��H+��������NaHSO3���ᷢ����Ӧ4HSO3-+Cl2=SO42-+2Cl-+3SO2��+2H2O�����ɶ����������壮
��� �⣺��1��Ư������Ч�ɷ��Ǵ�����ƣ����������Ũ���ᷴӦ�ķ�Ӧ����ʽΪ��Ca��ClO��2+4HCl��Ũ���TCaCl2+2Cl2��+2H2O��
�ʴ�Ϊ��Ca��ClO��2��Ca��ClO��2+4HCl��Ũ���TCaCl2+2Cl2��+2H2O��
��2�������ӷ�����Ӧ��ȡ�������к����Ȼ��⣬�Ȼ���������ˮ�������ڱ���ʳ��ˮ���ܽ�Ȳ���Bװ�ÿ��Գ�ȥCl2��HCl��
װ��B���ǰ�ȫƿ�����ʵ�����ʱC���Ƿ�����������������ʱB�еģ�ѹǿ����B�г���©����Һ���������γ�ˮ����
�ʴ�Ϊ����ȥCl2��HCl��B�г���©����Һ���������γ�һ��ˮ������ƿ��Һ���½���
��3��װ��C��ʵ��Ŀ������֤�����Ƿ����Ư���ԣ���֤�����Ƿ����Ư���ԣ�Ҫ��֤����������Ư���ԣ�ʪ�����ɫ�����У�������ˮ��Ӧ���ɴ��������Ư���ԣ�ѡ����abc�Ģ��ж��Ǹ��������ͨ��ʪ�����ɫ����������֤������Ư���ԣ�����C��I��II��III���η���ʪ�����ɫ��������ˮ�Ȼ��ơ��������ɫ����������ѡd��
�ʴ�Ϊ��d��
��4�������������廯�Ʒ�Ӧ�����嵥�ʣ�Һ���嵥�ʺ͵⻯����Һ�еĵ⻯�ط�Ӧ���ɵⵥ�ʣ������������塢�ⵥ��֮����û���Ӧ�������ж��ȡ��塢��ķǽ�����ǿ����
�ʴ�Ϊ���Ƚ��ȡ��塢��ķǽ�����ǿ����
��5����������װ��D�к��嵥�ʵ�������Һ�����ʵ⻯�غͱ���װ��E�У��嵥�ʺ͵⻯�ط�Ӧ���ɵⵥ�ʣ��ⵥ�����ڱ����Ϻ�ɫ�����۲쵽�������ǣ�E����Һ��Ϊ���㣬�ϲ㣨���㣩Ϊ�Ϻ�ɫ��
�ʴ�Ϊ��E����Һ��Ϊ���㣬�ϲ㣨���㣩Ϊ�Ϻ�ɫ��
��6����������ǿ�����ԣ�����Һ�н�SO32-����SO42-ͬʱ����Cl-��H+����Ӧ���ӷ���ʽΪSO32-+Cl2+H2O=SO42-+2Cl-+2H+��������NaHSO3���ᷢ����ӦHSO3-+Cl2+H2O=SO42-+2Cl-+3H+��4HSO3-+Cl2=SO42-+2Cl-+3SO2��+2H2O�����ɶ����������壬����������Ⱦ���������Բ�����NaHSO3����Na2SO3��
�ʴ�Ϊ��HSO3-+Cl2+H2O=SO42-+2Cl-+3H+��4HSO3-+Cl2=SO42-+2Cl-+3SO2��+2H2O����
���� ���⿼��������ʵ������ȡ��������ѧ���ʡ�ʵ����ơ�ʵ��װ�õ��������ۡ���ѧ����ʽ����д�ȣ��Ƕ���ѧ֪ʶ���ۺ����ã�ע�����֪ʶ�����գ������Ѷ��еȣ�

| 0�� | 50�� | 80�� | |
| Ca��OH��2 | 0.173g | 0.13g | 0.094g |
| Ba��OH��2•8H2O | 1.64g | 13.2g | 101.4g |

��1������۱�ΪCaO��BaO�Ļ����ͨ�����ý�̿��Ϊ��Դ���Ӿ���Ч��ĽǶȿ��ǣ�����̿�۸�������⣬����һ����Ҫԭ�������ý�̿ȼ�ղ����ĸ���ʹ��ʯ�ֽ⣬�йط�ӦΪC+O2$\frac{\underline{\;��ȼ\;}}{\;}$CO2��CaCO3$\frac{\underline{\;����\;}}{\;}$CaO+CO2����BaCO3$\frac{\underline{\;����\;}}{\;}$BaO+CO2����������Ӧ���ɵĶ�����̼��������������ȡ����CaCO3��BaCO3��ԭ�ϣ�
��2���Լ�a��ˮ�������ƣ���������ľ�����������ǽ����Һ������80�棬����Ca��OH��2�����˵õ�Ca��OH��2�����Ba��OH��2��Һ��
��3���Լ�b���Լ�c�Ƿ���ͬһ���ʣ�����ǡ�����д�������Լ�c������Ӧ�����ӷ���ʽ��CO2+Ba2++2OH-=BaCO3��+H2O��
��2C2H8��g��+7O2��g��=6CO��g��+8H2O��l����H=-2741.8kJ/mol
��2CO��g��+O2��g��=2CO2��g����H=-566kJ/mol
��1����ӦC2H8��g��+5O2��g��=3CO2��g��+4H2O��l���ġ�H=-2219.9kJ/mol��
��2��C2H8�ڲ�������������ȼ�գ�����CO��CO2�Լ���̬ˮ�������еIJ���ͨ��һ���̶�������ܱ������У���һ�������·������¿��淴Ӧ��
CO��g��+H2O��g��?CO2��g��+H2��g��
��������ʵ��˵���÷�Ӧ�Դﵽƽ�����bd��
a����ϵ�е�ѹǿ��������Ӧ
b��v����H2��=v����CO��
c����������ƽ����Է����������ٷ����仯
d��CO2��Ũ�Ȳ��ٷ����仯
��T��ʱ����һ�������������ͨ��һ������CO��g����H2O��g����������Ӧ�������¶Ȳ��䣬������Ũ�ȱ仯���±���
| ʱ��/min | CO | H2O��g�� | CO2 | H2 |
| 0 | 0.200 | 0.300 | 0 | 0 |
| 2 | 0.138 | 0.238 | 0.062 | 0.062 |
| 3 | 0.100 | 0.200 | 0.100 | 0.100 |
| 4 | 0.100 | 0.200 | 0.100 | 0.100 |
| 5 | 0.116 | 0.216 | 0.084 | C1 |
| 6 | 0.096 | 0.266 | 0.104 | C2 |
��3�����ݣ�1���еķ�Ӧ�������һ������ȼ�ϵ�أ�һ��ͨ���������һ��ͨ��������壻ȼ�ϵ���ڲ������ڵIJ����������ƣ�Y2O3��������ﯣ�ZrO2�����壬�����ڲ����Դ���O2-���ڵ���ڲ�O2-���������������������صĸ�����ӦʽΪC3H8+10O2--20e-=3CO2+4H2O��
��4��������ȼ�ϵ�أ��ö��Ե�ص������Al��NO3��3��NaCl�Ļ����Һ���������У������������ܹ۲쵽�����������������ɣ����ɰ�ɫ���������ɫ�������ܽ⣮
| A�� | 20�� | B�� | 40�� | C�� | 48�� | D�� | 36�� |
| A�� | ���³�ѹ�£�48gO2��O3���е���ԭ������Ϊ3NA5.4g��������NaOH��Ӧת�Ƶĵ�����Ϊ0.3NA | |
| B�� | 12g��ˮ��D2O���к��еĵ�����Ϊ6 NA | |
| C�� | ��״���£�11.2L������ԭ����Ϊ6NA | |
| D�� | 160g��������ˮ�γ�1L��Һ����Һ�����ʵ���Ũ��Ϊ1mol/L |
| A�� | Ca��OH��2�TCa2++2OH- | B�� | �ƾ���CH3CH2OH�TCH3CH2O-+H+ | ||
| C�� | BaCl2�TBa2++Cl${\;}_{2}^{2-}$ | D�� | H2SO4$\frac{\underline{\;ͨ��\;}}{\;}$2H++SO${\;}_{4}^{2-}$ |