��Ŀ����
������Ԫ��A��B��C��D����������Ӧˮ����ֱ�ΪX��Y��Z��W��A�Ƕ�������ԭ�Ӱ뾶����Ԫ�أ�������X��Z��W������Y��Ӧ��A��C��D��ԭ��������0.1mol/L X��Z��W��Һ��pH��ͼ��ʾ����֪lg2=0.3��������˵����ȷ���ǣ�������

A. A�����Ӱ뾶С��B�����Ӱ뾶
B. W��X�����ʺ��еĻ�ѧ��������ͬ
C. D�⻯���ȶ���С��C�⻯���ȶ���
D. B�ļ����ӻ�Ӱ��ˮ�ĵ���ƽ��
����ƹ㷺����ʳƷ��������ʯ�͵ȹ�ҵ�����ϣ�300��400�����ҷֽ⡣
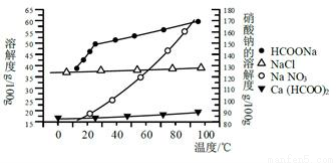
��ʵ������ȡ�ķ���֮һ�ǣ�Ca(OH)2 +2HCHO + H2O2 = Ca(HCOO)2 + 2H2O + H2����ʵ������ȡʱ������ҵ���������ƺͼ�ȩ���μ��뵽��������Ϊ30-70%�Ĺ���������Һ�У�Ͷ�����ʵ���֮������Ϊ1��2��1.2�������տɵõ���������98%�������ؽ����������͵����ʲ�Ʒ��
��1��������������������Զ࣬��Ŀ����__________��
��2����Ӧ�¶���ÿ�����30-70��֮�䣬�¶Ȳ����ߣ�����Ҫԭ����__________��
��3���Ʊ�ʱ�ڻ����Һ��Ҫ���������������Ƽ�ȩ��������Ӧ�⣬��Ҫ����������Na2S��Һ�������Ƶ�Ŀ����__________��
��4��ʵ��ʱ��ǿ������45min����Ŀ����__________���������������Һ��pH 7��8����Ŀ����__________����ᾧ���롢����ò�Ʒ��
��ij�о���ѧϰС���ù�ҵ̼���(��Ҫ�ɷ�ΪCaCO3������Ϊ��Al2O3��FeCO3) Ϊԭ�ϣ����Ʊ������Σ������������Һ�����ȡ����ơ������ͼ�������ʵ��ܽ������������ؽ������������������������pH(��ʼ������pH����������Ũ��Ϊ1.0 mol��L-1����)�����ṩ���Լ��У�A�������ƣ�B��5mol��L��1���ᣬc��5mol��L��1���ᣬd��5mol��L��1���ᣬe��3%H2O2��Һ��f.����ʯ��ˮ��
�������� | ��ʼ������pH | ������ȫ��pH |
Fe3�� | 1��1 | 3��2 |
Al3�� | 3��0 | 5��0 |
Fe2�� | 5��8 | 8��8 |
�벹��������̼����Ʊ�����Ƶ�ʵ�鲽�� ��
����1.��ȡ13.6g����������Լ20mLˮ������ܴ��ã�����ȡ��ϸ��̼�����Ʒ10g���á�
����2��_________��
����3��_________��
����4�����˺���Һ���������Һ��ϣ�������ҺpH 7��8����ֽ��裬������Һ������Ũ����__________��ϴ�ӡ�60��ʱ����ü���ƾ��塣
���и���ʵ��������������ó��Ľ�����ȷ����
ѡ�� | ʵ����������� | ���� |
A | �ⶨ�����ʵ���Ũ�ȵ�Na2CO3��Na2SO3��Һ��pH��ǰ��pH�Ⱥ��ߵĴ� | �ǽ����ԣ�S>C |
B | ����Һ�еμ�Na2CO3��Һ����Һ����� | CO32-�������������C6H5O-ǿ |
C | ��10 mL 0.2 mol��L-1NaOH��Һ�е���2��0.1 mol��L-1MgCl2��Һ��������ɫ�������ٵμ�2��0.1 mol��L-1FeCl3��Һ����ɫ����ת��Ϊ���ɫ���� | ��ͬ�¶��µ�Ksp��Mg(OH)2>Fe(OH)3 |
D | ��KI��FeCl3��Һ���Թ��л�Ϻ���CCl4�������ã��²���Һ���Ϻ�ɫ | Fe3+�������Դ���I2 |
A. A B. B C. C D. D




 Cr3+
Cr3+ Cr��OH��3��
Cr��OH��3�� 
