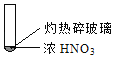题目内容
【题目】用MnO2和浓盐酸制取纯净干燥的氯气,并让氯气与铜粉反应制取纯净的无水CuCl2,装置如下图所示。
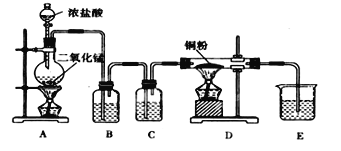
(1)B中选用的试剂是____________,其作用是__________;C中选用的试剂的作用是_________
(2)D中反应的化学方程式是_______________________
(3)某学生应用如图所示的方法研究物质的性质,其中气体X的主要成分是氯气。回答下列问题:
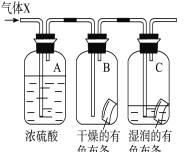
① 与研究目的直接相关的B、C中的实验现象是________。
② 如果通入气体中混有SO2,能否看到相同的现象? _________(填“能”、“不能”或者“”“不能确定”),用化学方程式进行解释: ______________________
③从物质性质的方面来看,这样的实验设计还存在事故隐患,事故表现是最后缺少一个____________装置,用化学方程式解释其原理__________________
【答案】 饱和食盐水 除HCl气体 浓H2SO4 ![]() B中无明显变化,C中有色布条褪色 不能 SO2+Cl2+2H2O=H2SO4+2HCl 尾气处理 2NaOH + Cl2 = NaCl + NaClO + H2O
B中无明显变化,C中有色布条褪色 不能 SO2+Cl2+2H2O=H2SO4+2HCl 尾气处理 2NaOH + Cl2 = NaCl + NaClO + H2O
【解析】(1)从A中制得的氯气含有杂质氯化氢、水蒸气,依次通过盛有饱和食盐水和浓硫酸的洗气瓶除去;故答案为:饱和食盐水;除去Cl2中的HCl;除去Cl2中的水蒸气;(2)氯气和铜在高温条件下化合生成氯化铜方程式为:Cu+Cl2![]() CuCl2;(3)① 与研究目的直接相关的B、C中的实验现象是B中无明显变化,C中有色布条褪色;② 如果通入气体中混有SO2,不能看到相同的现象,因为会发生反应SO2+Cl2+2H2O=H2SO4+2HCl,生成物没有漂白性;③从物质性质的方面来看,这样的实验设计还存在事故隐患,事故表现是最后缺少一个尾气处理装置,用化学方程式解释其原理2NaOH + Cl2 = NaCl + NaClO + H2O。
CuCl2;(3)① 与研究目的直接相关的B、C中的实验现象是B中无明显变化,C中有色布条褪色;② 如果通入气体中混有SO2,不能看到相同的现象,因为会发生反应SO2+Cl2+2H2O=H2SO4+2HCl,生成物没有漂白性;③从物质性质的方面来看,这样的实验设计还存在事故隐患,事故表现是最后缺少一个尾气处理装置,用化学方程式解释其原理2NaOH + Cl2 = NaCl + NaClO + H2O。

 直通贵州名校周测月考直通名校系列答案
直通贵州名校周测月考直通名校系列答案【题目】下述实验中均有红棕色气体产生,对比分析所得结论不正确的是( )
|
|
|
① | ② | ③ |
A. 由①中的红棕色气体,推断产生的气体一定是混合气体
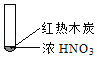
B. 红棕色气体不能表明②中木炭与浓硝酸产生了反应
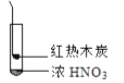
C. 由③说明浓硝酸具有挥发性,生成的红棕色气体为还原产物
D. ③的气体产物中检测出CO2,由此说明木炭一定与浓硝酸发生了反应
【题目】(14分)
研究小组用下图装置制取Cl2,证明产生的气体中含有HCl。
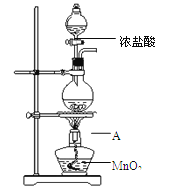
(1)仪器A的名称为 ;A中反应的离子方程式为 。
(2)甲同学将A中产生的气体通入下列溶液:
实验序号 | 试剂 | 现象 |
a | 紫色石蕊溶液 |
|
b | AgNO3溶液 | 出现白色沉淀 |
①实验a中的现象为 。
②不能证明产生的气体中含有HCl的实验是 (填字母序号)。
(3)已知将HCl气体通入饱和食盐水中有白色固体析出。乙同学将A中产生的气体通入饱和食盐水中,有白色固体析出,但该实验不能证明气体中含有HCl,结合化学用语解释其原因: 。
(4)已知:2S2O32- + I2 === S4O62- + 2I-。丙同学将A中产生的气体通入蒸馏水中,得到溶液X,进行以下实验证明气体中含有HCl。
I.测定X中溶解的Cl2。取25.00 mL溶液X,加入过量KI溶液,然后用0.04 molL-1 Na2S2O3溶液滴定生成的I2,达滴定终点时消耗Na2S2O3溶液V mL。
II.测定X中Cl元素总量。另取25.00 mL溶液X,选用适当的还原剂将溶解的Cl2全部还原为Cl-,再用0.10 molL-1 AgNO3溶液滴定所得溶液中的Cl-。
X中的HClO不会影响I的测定结果,原因是 。
由I、II 中实验数据可证明A中产生的气体中含有HCl,则II中消耗0.10 molL-1 AgNO3溶液的体积应大于 mL(用含V的代数式表示)。