题目内容
( 10分)有X、Y、Z三种元素,已知:①X2-、Y-均与Y的气态氢化物分子具有相同的电子数;②Z与Y可组成化合物ZY3,ZY3溶液遇苯酚呈紫色。 请回答:
(1)Y的最高价氧化物对应水化物的化学式是____________
(2)将ZY3溶液滴入沸水可得到红褐色液体,反应的离子方程式是________________________,此液体具有的性质是__________________(填写序号字母)。
a.光束通过该液体时形成光亮的“通路”?
b.插入电极通直流电后,有一极附近液体颜色加深?
c.向该液体中加入硝酸银溶液,无沉淀产生?
d.将该液体加热、蒸干、灼烧后,有氧化物生成?
(3)X单质在空气中燃烧生成一种无色有刺激性气味的气体。?
①已知一定条件下,每1 mol该气体被O2氧化放热98.0 kJ。若2 mol该气体与1 mol O2在此条件下发生反应,达到平衡时放出的热量是176.4 kJ,则该气体的转化率为_________________________
②原无色有刺激性气味的气体与含1.5 mol Y的一种含氧酸(该酸的某盐常用于实验室制取氧气)溶液在一定条件下反应,可生成一种强酸和一种氧化物。若有1.5×6.02×1023个电子转移时,该反应的化学方程式是____________________________
(1)Y的最高价氧化物对应水化物的化学式是____________
(2)将ZY3溶液滴入沸水可得到红褐色液体,反应的离子方程式是________________________,此液体具有的性质是__________________(填写序号字母)。
a.光束通过该液体时形成光亮的“通路”?
b.插入电极通直流电后,有一极附近液体颜色加深?
c.向该液体中加入硝酸银溶液,无沉淀产生?
d.将该液体加热、蒸干、灼烧后,有氧化物生成?
(3)X单质在空气中燃烧生成一种无色有刺激性气味的气体。?
①已知一定条件下,每1 mol该气体被O2氧化放热98.0 kJ。若2 mol该气体与1 mol O2在此条件下发生反应,达到平衡时放出的热量是176.4 kJ,则该气体的转化率为_________________________
②原无色有刺激性气味的气体与含1.5 mol Y的一种含氧酸(该酸的某盐常用于实验室制取氧气)溶液在一定条件下反应,可生成一种强酸和一种氧化物。若有1.5×6.02×1023个电子转移时,该反应的化学方程式是____________________________
(1)HClO4 (2)Fe3++3H2O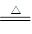 Fe(OH)3(胶体)+3H+ a、b、d
Fe(OH)3(胶体)+3H+ a、b、d
(3)①90% ②SO2+2HClO3===H2SO4+2ClO2
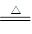 Fe(OH)3(胶体)+3H+ a、b、d
Fe(OH)3(胶体)+3H+ a、b、d(3)①90% ②SO2+2HClO3===H2SO4+2ClO2
试题分析:(1)ZY3溶液遇苯酚呈紫色,说明Z是Fe,Y是Cl。X2-、Y-均与Y的气态氢化物分子具有相同的电子数,所以X是S。氯元素的最高价是+7价,所以Y的最高价氧化物对应水化物的化学式是HClO4。
(2)将氯化铁溶液滴入沸水可得到红褐色液体,这是实验室制备氢氧化铁胶体的,因此该分散系属于胶体,反应的离子方程式是Fe3++3H2O
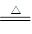 Fe(OH)3(胶体)+3H+。胶体具有丁达尔效应,能发生电泳选项,与能发生聚沉,且生成的氢氧化铁固体受热可以分解生成氧化铁和水,所以选项a、b、d都是正确的,c不正确,答案选abd。
Fe(OH)3(胶体)+3H+。胶体具有丁达尔效应,能发生电泳选项,与能发生聚沉,且生成的氢氧化铁固体受热可以分解生成氧化铁和水,所以选项a、b、d都是正确的,c不正确,答案选abd。(3)①根据反应热可知,参加反应的SO2的物质的量是176.4 kJ÷98.0 kJ/mol=1.8mol,所以SO2的转化率是1.8mol÷2mol=90%。
②该酸的某盐常用于实验室制取氧气,所以该盐是氯酸钾。转移电子的物质的量是1.5mol,这说明在反应中氯酸钾得到1个电子,因此氯酸钾的还原产物中氯元素的化合价是+4价,则应该是ClO2,所以该反应的化学方程式是SO2+2HClO3===H2SO4+2ClO2。
点评:该题属于中等浓度的试题,主要考查学生对常见基础知识的掌握程度,以及灵活运用知识解决实际问题的能力。关于对热化学方程式和焓变的理解、计算,以及氧化还原反应的有关计算并不麻烦。化学计算的实质是用数学工具处理化学问题,不仅能考查学生利用化学知识解决化学问题能力,而且还能考查学生的形象思维能力。

练习册系列答案
 鸿图图书寒假作业假期作业吉林大学出版社系列答案
鸿图图书寒假作业假期作业吉林大学出版社系列答案
相关题目