��Ŀ����
��֪��ӦAsO43����2I����2H�� AsO33��
AsO33�� ��I2��H2O�ǿ��淴Ӧ�������ͼװ�ã�C1��C2��Ϊʯī�缫�����ֱ��������������
��I2��H2O�ǿ��淴Ӧ�������ͼװ�ã�C1��C2��Ϊʯī�缫�����ֱ��������������

����B�ձ�����μ���Ũ����
����B�ձ�����μ���40% NaOH��Һ
������ֵ�����ָ�������ƫת���ݴˣ������ж���ȷ����
A������������У�C2���Ϸ����ķ�ӦΪ��AsO43����2H����2e��=AsO33����H2O
B������������У������е�K������B�ձ���Һ
C������������У�C1Ϊ����
D������������У�C1���Ϸ����ķ�ӦΪ��2I��_2e��=I2
 ��У����ϵ�д�
��У����ϵ�д�ij�о���ѧϰС���������ռ�����Ϣ���ء��ơ��ơ�þ�Ȼ��ý���������CO2������ȼ�ա����Ƕ�����CO2������ȼ�պ�IJ����еİ�ɫ���ʽ���������̽����
��ʵ�顿��ȼ�յ���Ѹ������ʢ��CO2�ļ���ƿ�У��������м���ȼ�գ���Ӧ����ȴ��ƿ���ź�ɫ������ƿ����ճ���Ű�ɫ���ʡ�
��1��ͨ������CO2������ȼ�յ�ʵ�飬����Ϊȼ�յ������ǣ� ��
��2��ȼ�յı����� ��
��3��2010��8�³������Ķ���˹ɭ�ִ����Ż���������е������Ҫ����ɭ�ֻ��������������⡣����ȼ�յ��������������Ϊʲô����ɭ�ַ�����������Ч��ֹɭ�ֻ��ֵ����� _��
��������衿
����1����ɫ������Na2O
����2����ɫ������Na2CO3
����3����ɫ������Na2O��Na2CO3�Ļ����
�����ʵ�鷽������֤���衿��С���ȼ�պ�İ�ɫ�����������̽����
ʵ�鷽�� | ʵ����� | ʵ������ | ���� |
����1 | ȡ������ɫ�������Թ��У���������ˮ������Ʒȫ������ˮ�������м�����ɫ��̪��Һ | ��Һ��ɺ�ɫ | ��ɫ����ΪNa2O |
����2 | ��ȡ������ɫ�������Թ��У���������ˮ������Ʒȫ������ˮ�������м��������CaCl2��Һ | ���ְ�ɫ���� | |
�ھ���Ƭ�̣�ȡ�ϲ���Һ���Թ��У��μ���ɫ��̪��Һ | ���������� |
��˼���뽻����
��4����ͬѧ��Ϊ�ɷ���1�ó����۲����ܣ������ԭ�� ��
��5����ͬѧ��Ϊ����2�õ��Ľ�����ȷ����ɫ����Ϊ ��
��6��ͨ������1�ͷ���2��ʵ�飬����Ϊ�������������У� ��������������� ��
��7�����ڶ�����̼��ȼ�յĻ�ѧ����ʽΪ ��
��8����ͬѧ��Ϊ��ɫ�����п������������ơ����Ƿ�ͬ���ͬѧ�Ĺ۵㣬���������� ��
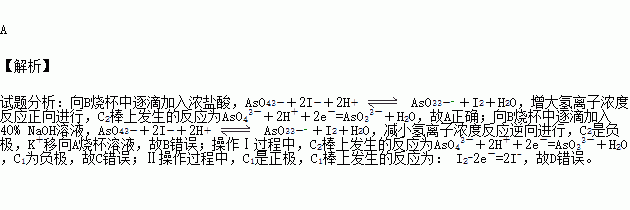

 A��OH��
A��OH�� H3O+ + OH��,��Һ̬NH3����ķ���ʽ��________________
H3O+ + OH��,��Һ̬NH3����ķ���ʽ��________________ ��3������0.10 mol•L-1����ͭ��Һ��ͨ�����H2S���壬ʹCu2+��ȫ����ΪCuS����ʱ��Һ�е�H+Ũ���� ����0.10 mol•L-1����ͭ��Һ�м�����������ϡ��Һ��ֽ�����dz��ɫ������ͭ�������ɣ�����Һ��pH=8ʱ��c��Cu2+��=___________(��֪Ksp[Cu(OH) 2]=2.2x10-20����
��3������0.10 mol•L-1����ͭ��Һ��ͨ�����H2S���壬ʹCu2+��ȫ����ΪCuS����ʱ��Һ�е�H+Ũ���� ����0.10 mol•L-1����ͭ��Һ�м�����������ϡ��Һ��ֽ�����dz��ɫ������ͭ�������ɣ�����Һ��pH=8ʱ��c��Cu2+��=___________(��֪Ksp[Cu(OH) 2]=2.2x10-20���� �����б�����ȷ����
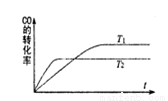
�����б�����ȷ���� CH3OH(g)����ͼ�Ǹ÷�Ӧ�ڲ�ͬ�¶���CO��ת������ʱ��仯�����ߡ������ж���ȷ���� �� ��
CH3OH(g)����ͼ�Ǹ÷�Ӧ�ڲ�ͬ�¶���CO��ת������ʱ��仯�����ߡ������ж���ȷ���� �� ��