题目内容
A、B两种有机物组成的混合物,当混合物的总质量相等时,无论A、B两种有机物以何种比例混合,完全燃烧后生成的二氧化碳质量都相等,符合这一条件的有机物组合是
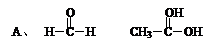
B、C6H6 C6H5OH
C、CH3OH HOCH2CH2OH D、CH4 C10H8O2
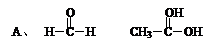
B、C6H6 C6H5OH
C、CH3OH HOCH2CH2OH D、CH4 C10H8O2
AD
据题意,完全燃烧后生成的CO2的质量相等,则要求两物质中碳元素的质量分数相同。
A、CH2O与C2H4O2,含碳元素质量分数相同
B、C6H6与C6H6O,含碳元素质量分数不同
C、CH4O与C2H6O2,含碳元素质量分数不同
D、CH4中含1个碳原子同时含4个氢原子,C10H8O2中可将2个氧原子的质量看作32个氢原子的质量,则可视为含有10个碳原子同时含有40个氢原子,即含碳元素的质量分数相同
故本题答案为A、D。
A、CH2O与C2H4O2,含碳元素质量分数相同
B、C6H6与C6H6O,含碳元素质量分数不同
C、CH4O与C2H6O2,含碳元素质量分数不同
D、CH4中含1个碳原子同时含4个氢原子,C10H8O2中可将2个氧原子的质量看作32个氢原子的质量,则可视为含有10个碳原子同时含有40个氢原子,即含碳元素的质量分数相同
故本题答案为A、D。

练习册系列答案
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案
相关题目