题目内容
【题目】亚磷酸二乙酯[HPO(OC2H5)2]是一种液态阻燃增塑剂。实验室采用PCl3和无水乙醇制备高纯度亚磷酸二乙酯,反应方程式为:PCl3 + 4C2H5OH → HPO(OC2H5)2 + HCl↑+2C2H5Cl + H2O;实验步骤如下:

①将45 mL CHCl3和46.00 g(1.0 mol)无水乙醇混合后加入250 mL三颈烧瓶中。
②从仪器A中滴加20 mL CHCl3和41.25 g (0.3 mol)PCl3混合溶液,用冰水控温6~8℃,开动搅拌器,约1 h滴加完毕。
③将反应物倒入烧杯中,用10%的Na2CO3溶液调节pH至7~8,再用去离子水洗涤三次,在仪器B中分离。
④减压蒸馏,收集产品,得29.60 g产品。
(1)装置图中仪器A为恒压滴液漏斗,其中支管的作用为______;倒置漏斗的作用为______;步骤③中仪器B名称为______。
(2)用碳酸钠溶液洗涤的目的是为了除去酸性物质______(填化学式)以及PCl3;
(3)从无水乙醇利用角度计算,本次实验产率为______(填数值)。
【答案】平衡压强,便于液体顺利滴下 防倒吸 分液漏斗 HCl 85.80%(85%—86%均可)
【解析】
仪器A为恒压滴液漏斗,有利于平衡压强,液体能顺利流入到三颈烧瓶中发生反应,将反应物放在三颈烧瓶中发生反应生成HPO(OC2H5)2 、 HCl、C2H5Cl,再制备过程中冰水控制温度,反应后将混合物倒入到盛有碳酸钠溶液的烧杯中洗涤HCl以及PCl3,再用分液漏斗分开亚磷酸二乙酯,根据反应物量计算理论产量,再计算产率。
⑴装置图中仪器A为恒压滴液漏斗,支管上面连接分液漏斗,下面连接三颈烧瓶,使得分液漏斗和三颈烧瓶大气相通,因此支管的作用为平衡压强,便于液体顺利滴下,由于该反应会产生HCl气体,HCl气体极易溶于水,进入到烧杯中,因此倒置漏斗的作用为_防倒吸,制得的亚磷酸二乙酯不溶于水,因此步骤③中仪器B名称为分液漏斗,故答案为:平衡压强,便于液体顺利滴下;防倒吸;分液漏斗;
⑵反应生成了盐酸、亚磷酸二乙酯和C2H5Cl,因此用碳酸钠溶液洗涤的目的是为了除去酸性物质HCl以及PCl3,故答案为:HCl;
⑶从无水乙醇利用角度计算,本次实验产率为______(填数值)。
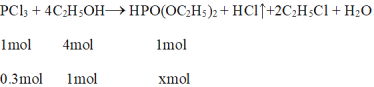
根据上面分析得出PCl3过量,应该按照C2H5OH的量来进行计算,得式子
![]() ,解得x = 0.25mol,
,解得x = 0.25mol,
本次实验产率![]() ,故答案为85.80%。
,故答案为85.80%。

 阅读快车系列答案
阅读快车系列答案【题目】某校化学实验课上,老师要求学生用硫酸铜溶液与氢氧化钠溶液制备Cu(OH)2,为了缩短实验时间,老师让学生将反应容器放在沸水浴中进行反应,结果出现了如下两种不同的实验现象:
操作 | 现象 | |
实验一 | 向NaOH溶液中滴加CuSO4溶液 | 黑色沉淀 |
实验二 | 向CuSO4溶液中滴加NaOH溶液 | 蓝色沉淀 |
(1)甲同学认为实验一中产生的黑色沉淀是___(填化学式),理由是___。
(2)为验证推测结果是否正确,甲同学将黑色沉淀过滤、洗涤、干燥后称得质量为ag,并按照如图所示装置进行实验,实验前后称得干燥管E的质量分别为cg和dg。

为确保实验的准确性,甲同学认为应在装置A反应一段时间后再接上装置E,点燃D中的酒精灯,其理由是___。乙同学认为甲同学的装置仍有不足,应在E的末端连接一个气囊,气囊的作用有两个:___。甲同学改进实验装置后完成实验,若a、c、d满足关系式:___,则证明甲同学对黑色沉淀的推测是正确的。
(3)丙同学认为实验二中的蓝色沉淀应为Cu(OH)2,丁同学立即提出反对意见,认为该蓝色沉淀一定不是Cu(OH)2。为确认实验二中蓝色沉淀的成分,丁同学从实验时药品的加入顺序考虑,可能是反应物的用量不同导致产物的不同,并上网查阅资料知,当NaOH溶液少量时会生成碱式硫酸铜[Cu2(OH)2SO4],反应的离子方程式为___。
(4)进一步查阅资料可知碱式硫酸铜为蓝色物质,难溶于水、可溶于酸。请你设计实验,验证实验二中生成的蓝色沉淀含有SO42-:___。