题目内容
16.(1)利用SiO2的化学性质,写出实现下列变化的化学方程式.SiO2→硅酸SiO2+2NaOH═Na2SiO3+H2ONa2SiO3+2HCl═H2SiO3↓+2NaCl
SiO2→高纯度的硅SiO2+2C$\frac{\underline{\;高温\;}}{\;}$Si(粗硅)+2CO2↑
Si(粗硅)+2Cl2$\frac{\underline{\;高温\;}}{\;}$SiCl4
SiCl4+2H2$\frac{\underline{\;高温\;}}{\;}$Si+4HCl
(2)实验室中盛放强碱(氢氧化钠)溶液的玻璃试剂瓶不能用玻璃塞,试说明原因:玻璃的主要成分是SiO2,它与强碱(NaOH)反应生成的Na2SiO3是一种黏结剂,能使瓶口和塞子粘结在一起..
分析 (1)二氧化硅与氢氧化钠反应生成硅酸钠和水,硅酸钠与盐酸反应生成氯化钠和硅酸;
二氧化硅与碳反应生成硅和一氧化碳,硅与氯气反应生成四氯化硅,四氯化硅被氢气还原生成硅和氯化氢;
(2)依据二氧化硅为酸性氧化物,能够与氢氧化钠反应生成硅酸钠溶液,硅酸钠具有粘性解答.
解答 解:(1)二氧化硅与氢氧化钠反应生成硅酸钠和水,硅酸钠与盐酸反应生成氯化钠和硅酸,化学方程式:SiO2+2NaOH═Na2SiO3+H2O Na2SiO3+2HCl═H2SiO3↓+2NaCl;
故答案为:SiO2+2NaOH═Na2SiO3+H2O Na2SiO3+2HCl═H2SiO3↓+2NaCl;
(2)二氧化硅与碳反应生成硅和一氧化碳,硅与氯气反应生成四氯化硅,四氯化硅被氢气还原生成硅和氯化氢,发生反应方程式为:SiO2+2C$\frac{\underline{\;高温\;}}{\;}$Si(粗硅)+2CO2↑;Si(粗硅)+2Cl2$\frac{\underline{\;高温\;}}{\;}$SiCl4;SiCl4+2H2$\frac{\underline{\;高温\;}}{\;}$Si+4HCl;
故答案为:SiO2+2C$\frac{\underline{\;高温\;}}{\;}$Si(粗硅)+2CO2↑;Si(粗硅)+2Cl2$\frac{\underline{\;高温\;}}{\;}$SiCl4;SiCl4+2H2$\frac{\underline{\;高温\;}}{\;}$Si+4HCl;
(2)玻璃的主要成分是SiO2,它与强碱(NaOH)反应生成的Na2SiO3是一种黏结剂,能使瓶口和塞子粘结在一起,所以实验室中盛放强碱(氢氧化钠)溶液的玻璃试剂瓶不能用玻璃塞;
故答案为:玻璃的主要成分是SiO2,它与强碱(NaOH)反应生成的Na2SiO3是一种黏结剂,能使瓶口和塞子粘结在一起.
点评 本题考查了化学方程式书写,明确硅及其化合物性质是解题关键,注意粗硅提纯及碱液的保存,题目难度不大.

 阅读快车系列答案
阅读快车系列答案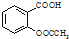 )是世界上应用最广泛的解热、镇痛和抗炎药.乙酰水杨酸受热易分解,分解温度为128~135℃.某学习小组在实验室以水杨酸(邻羟基苯甲酸)与醋酸酐[(CH3CO)2O]为主要原料合成阿司匹林,制备基本操作流程如下:
)是世界上应用最广泛的解热、镇痛和抗炎药.乙酰水杨酸受热易分解,分解温度为128~135℃.某学习小组在实验室以水杨酸(邻羟基苯甲酸)与醋酸酐[(CH3CO)2O]为主要原料合成阿司匹林,制备基本操作流程如下:
主要试剂和产品的物理常数
| 名称 | 相对分子质量 | 熔点或沸点 (℃) | 水 |
| 水杨酸 | 138 | 158(熔点) | 微溶 |
| 醋酸酐 | 102 | 139.4(沸点) | 反应 |
| 乙烯水杨酸 | 180 | 135(熔点) | 微溶 |
(1)制备阿司匹林时,要使用干燥的仪器的原因是防止乙酸酐水解.
(2)合成阿斯匹林时,最合适的加热方法是水浴加热.
(3)提纯粗产物中加入饱和NaHCO3溶液至没有CO2产生为止,再抽滤,则加饱和NaHCO3溶液的目的是使乙酰水杨酸与NaHCO3溶液作用转化为易溶于水的乙酰水杨酸钠,便于与聚合物分离.
另一种改进的提纯方法,称为重结晶提纯法.方法如下:

(4)改进的提纯方法中加热回流的装置如图所示

①使用温度计的目的是控制反应温度,防止温度过高,乙酰水杨酸受热分解.冷凝水的流进方向是b.(填“b”或“c”).
②重结晶提纯法所得产品的有机杂质要比原方案少的原因水杨酸易溶于乙酸乙酯,冷却结晶时大部分水杨酸仍溶解在乙酸乙酯中很少结晶出来.
(5)检验产品中是否含有水杨酸的化学方法是取少量结晶于试管中,加蒸馏水溶解,滴加FeCl3溶液,若呈紫蓝色,则含水杨酸.
(6)该学习小组在实验中原料用量:2.0g水杨酸、5.0mL醋酸酐(ρ=1.08g/cm3),最终称得产品m=2.2g,则所得乙酰水杨酸的产率为84.3%.
| A. | 在水溶液中或熔融状态下能导电的物质 | |
| B. | 凡在水中能生成离子因而能导电的物质 | |
| C. | 氧化钠溶于后水溶液能导电,但溶液中的离子并非本身电离,因而氧化钠是非电解质 | |
| D. | 在水溶液里或熔融状态下本身能电离出阳离子和阴离子,因而是能导电的化合物 |
| A. | Na+H2O | B. | Fe+H2O(g) | C. | CO2+H2O | D. | Na2O2+H2O |
| A. | 2.8g | B. | 5.6g | C. | 8.4g | D. | 16.8g |
| A. | 35Cl原子所含质子数为18 | |
| B. | $\frac{1}{18}$ mol的1H35Cl分子所含中子数约为6.02×1023 | |
| C. | 3.5 g的35Cl2气体的体积为2.24 L | |
| D. | 35Cl2气体的摩尔质量为70 g•mol-1 |