题目内容
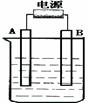
在如下图用石墨作电极的电解池中,放入500 mL含一种溶质的某蓝色溶液进行电解,观察到A电极表面有红色的固态物质生成,B电极有无色气体生成;当溶液中的原有溶质完全电解后,停止电解,取出A电极,洗涤、干燥、称量,电极增重1.6 g。请回答下列问题。 
(1)B电极发生反应的电极反应式 ___________________ 。
(2)写出电解时反应的离子方程式 ___________________ 。
(3)电解后溶液的pH为________,要使电解后溶液恢复到电解前的状态,则需加入__________,其质量为__________。(假设电解前后溶液的体积不变)
(4)请你设计实验确定原溶液中可能所含的酸根离子,要求:提出两种可能的假设,分别写出论证这两种假设的操作步骤、实验现象和实验结论。
①假设一:__________________________________________________________;
②假设二:__________________________________________________________。
解析:根据蓝色溶液和红色固体判断电解的是含Cu2+的溶液。再根据A极质量增加,B极产生无色气体判断A为阴极,B为阳极,电极反应式分别为:2Cu2++4e-====2Cu,4OH--4e-====2H2O+O2↑
电解后:c(H+)=2c(Cu2+)=![]() =0.1 mol·L-1
=0.1 mol·L-1
所以pH=1
根据电解方程式:2Cu2++2H2O![]() 2Cu+O2↑+4H+,可知从溶液中析出的是Cu和O2,比例为2∶1,相当于CuO,因此应向溶液中加入CuO,其质量为
2Cu+O2↑+4H+,可知从溶液中析出的是Cu和O2,比例为2∶1,相当于CuO,因此应向溶液中加入CuO,其质量为![]() ×80 g·mol-1=2 g,才能恢复到原状态。第(4)步中,可以假设阴离子为
×80 g·mol-1=2 g,才能恢复到原状态。第(4)步中,可以假设阴离子为![]() 、
、![]() ,但是不能为Cl-,因为阳极产生的是无色无味气体。
,但是不能为Cl-,因为阳极产生的是无色无味气体。
答案:(1)4OH--4e-====2H2O+O2↑
(2)2Cu2++2H2O![]() 2Cu+O2↑+4H+ (3)1 CuO 2 g
2Cu+O2↑+4H+ (3)1 CuO 2 g
(4)①假设原溶液中的酸根离子为![]() 。取电解后的溶液向其中加入BaCl2溶液,若有白色沉淀产生,则原溶液中含
。取电解后的溶液向其中加入BaCl2溶液,若有白色沉淀产生,则原溶液中含![]()
②假设原溶液中的酸根离子为![]() 。取电解后的溶液,向其中加入Cu微热,若Cu溶解,并有无色气体生成,在空气中变为红棕色,则含有
。取电解后的溶液,向其中加入Cu微热,若Cu溶解,并有无色气体生成,在空气中变为红棕色,则含有![]() 。
。


 方程式
方程式  。
。