题目内容
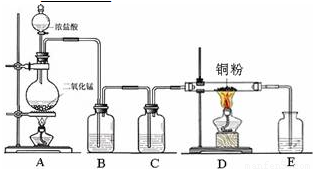 实验室里用下、如图所示装置制取纯净的无水CuCl2.试回答下列问题:
实验室里用下、如图所示装置制取纯净的无水CuCl2.试回答下列问题:(1)写出烧瓶中发生反应的化学方程式,并标出电子转移的方向和数目 .
(2)B处盛有饱和食盐水(或水),其作用是 .
(3)C处盛放的试剂 (填名称),其作用是 .
(4)E处盛有 (填名称),发生反应的离子方程式为 .
(5)实验结束时,应先熄灭 处酒精灯.
【答案】分析:(1)A为制备氯气装置,装置A中反应为二氧化锰与盐酸反应生成氯化锰、氯气、水.根据化合价变化标出电子转移的方向和数目;
(2)(3)制纯净干燥的氯气,要除去混在氯气中的氯化氢和水蒸气.除去氯化氢气体用饱和食盐水(或水),除去水蒸气用浓硫酸.应先除氯化氢,后干燥;
(4)尾气中含有氯气,污染环境,用氢氧化钠溶液吸收,氯气与氢氧化钠反应生成氯化钠、次氯酸钠与水;
(5)根据防止倒吸解答.
解答:解:(1)A为制备氯气装置,装置A中反应为二氧化锰与盐酸反应生成氯化锰、氯气、水,反应方程式为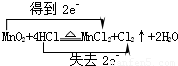 ,
,
故答案为: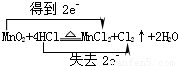 ;
;
(2)浓盐酸具有挥发性,所以制备的氯气中含有氯化氢,氯化氢极易溶于水,氯气的溶解度较小,所以可用饱和食盐水(或水)除去氯气气体中的氯化氢,
故答案为:除去Cl2中的HCl;
(3)因为题中要求制取纯净的无水CuCl2,所以要除去氯气中混有的水蒸气,且不引进新的杂质,氯气也和该物质不反应,所以选择浓硫酸干燥,
故答案为:浓硫酸;干燥Cl2;
(4)尾气中含有氯气,氯气有毒,污染环境,不能直接排放到大气中.常用氢氧化钠溶液吸收,氯气与氢氧化钠反应生成氯化钠、次氯酸钠与水,反应离子方程式为
Cl2+2OH-=Cl-+ClO-+H2O,故答案为:氢氧化钠溶液;Cl2+2OH-=Cl-+ClO-+H2O;
(5)为防止倒吸应先熄灭D的酒精灯,冷却再熄灭A的酒精灯,故答案为:D.
点评:本题有一定的综合性,把氯气的实验室制法和氯气的化学性质结合起来.考查学生对实验原理、实验装置的理解、物质的制备与性质,难度中等,实验室制取氯气的注意事项:1、必须用浓盐酸,稀盐酸不反应.2、为了减少制得的氯气中氯化氢的含量,所以加热温度不宜过高,浓盐酸具有挥发性.3、实验结束后,先使反应停止并排出残留的氯气,再拆卸装置,避免污染空气.4、尾气吸收时,不能用澄清石灰水吸收氯气,因为溶液中含有氢氧化钙的量少,吸收不完全.
(2)(3)制纯净干燥的氯气,要除去混在氯气中的氯化氢和水蒸气.除去氯化氢气体用饱和食盐水(或水),除去水蒸气用浓硫酸.应先除氯化氢,后干燥;
(4)尾气中含有氯气,污染环境,用氢氧化钠溶液吸收,氯气与氢氧化钠反应生成氯化钠、次氯酸钠与水;
(5)根据防止倒吸解答.
解答:解:(1)A为制备氯气装置,装置A中反应为二氧化锰与盐酸反应生成氯化锰、氯气、水,反应方程式为
 ,
,故答案为:
 ;
;(2)浓盐酸具有挥发性,所以制备的氯气中含有氯化氢,氯化氢极易溶于水,氯气的溶解度较小,所以可用饱和食盐水(或水)除去氯气气体中的氯化氢,
故答案为:除去Cl2中的HCl;
(3)因为题中要求制取纯净的无水CuCl2,所以要除去氯气中混有的水蒸气,且不引进新的杂质,氯气也和该物质不反应,所以选择浓硫酸干燥,
故答案为:浓硫酸;干燥Cl2;
(4)尾气中含有氯气,氯气有毒,污染环境,不能直接排放到大气中.常用氢氧化钠溶液吸收,氯气与氢氧化钠反应生成氯化钠、次氯酸钠与水,反应离子方程式为
Cl2+2OH-=Cl-+ClO-+H2O,故答案为:氢氧化钠溶液;Cl2+2OH-=Cl-+ClO-+H2O;
(5)为防止倒吸应先熄灭D的酒精灯,冷却再熄灭A的酒精灯,故答案为:D.
点评:本题有一定的综合性,把氯气的实验室制法和氯气的化学性质结合起来.考查学生对实验原理、实验装置的理解、物质的制备与性质,难度中等,实验室制取氯气的注意事项:1、必须用浓盐酸,稀盐酸不反应.2、为了减少制得的氯气中氯化氢的含量,所以加热温度不宜过高,浓盐酸具有挥发性.3、实验结束后,先使反应停止并排出残留的氯气,再拆卸装置,避免污染空气.4、尾气吸收时,不能用澄清石灰水吸收氯气,因为溶液中含有氢氧化钙的量少,吸收不完全.

练习册系列答案
 举一反三同步巧讲精练系列答案
举一反三同步巧讲精练系列答案 口算与应用题卡系列答案
口算与应用题卡系列答案 名师点睛字词句段篇系列答案
名师点睛字词句段篇系列答案
相关题目
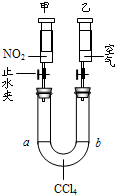 (1)下列关于实验操作的叙述中正确的为
(1)下列关于实验操作的叙述中正确的为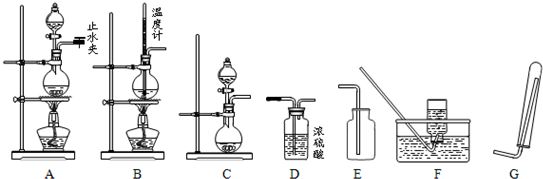
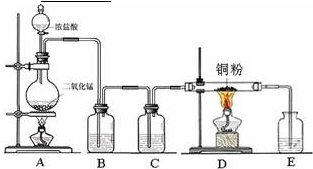 实验室里用下、如图所示装置制取纯净的无水CuCl2.试回答下列问题:
实验室里用下、如图所示装置制取纯净的无水CuCl2.试回答下列问题: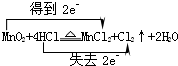
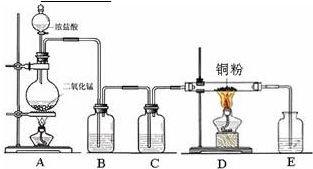 实验室里用下、如图所示装置制取纯净的无水CuCl2.试回答下列问题:
实验室里用下、如图所示装置制取纯净的无水CuCl2.试回答下列问题: