题目内容
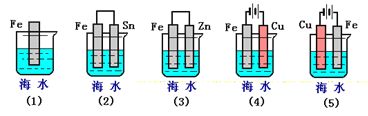
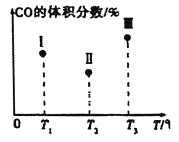
【题目】一定条件下Fe2O3可被甲烷还原为“纳米级”的金属铁,其反应:Fe2O3(s)+3CH4(g)2Fe(s)+3CO(g)+6H2(g) ΔH,在容积固定且均为1L的Ⅰ、Ⅱ、Ⅲ三个相同密闭容器中加入足量“纳米级”的金属铁,然后分别充入1molCO和2molH2,三个容器的反应温度分别为T1、T2、T3(依次升高)且恒定不变,测得反应均进行到t min时CO的体积分数如图所示。下列说法正确的是( )
A.该反应的ΔH>0
B.容器Ⅲ中CO的体积分数可能为35%
C.容器中固体的质量不再改变,不能说明反应已达平衡状态
D.反应进行到tmin时,三个容器中一定达到平衡状态的是Ⅱ和Ⅲ
【答案】A
【解析】
在容积均为1L的Ⅰ、Ⅱ、Ⅲ三个相同密闭容器中加入足量“纳米级”的金属铁,然后分别充入1molCO和2molH2,发生反应Fe2O3(s)+3CH4(g)2Fe(s)+3CO(g)+6H2(g) ![]() ,根据图中Ⅰ、Ⅱ、ⅢCO的体积分数由小到大依次为:Ⅱ
,根据图中Ⅰ、Ⅱ、ⅢCO的体积分数由小到大依次为:Ⅱ![]() Ⅰ
Ⅰ![]() Ⅲ,
Ⅲ,![]() 中的状态转变成
中的状态转变成![]() 中的状态,CO百分含量减小,说明反应逆向进行,说明
中的状态,CO百分含量减小,说明反应逆向进行,说明![]() 未达平衡状态,
未达平衡状态,![]() 中的状态转变成
中的状态转变成![]() 中的状态,CO百分含量增大,说明反应正向进行,说明
中的状态,CO百分含量增大,说明反应正向进行,说明![]() 可能达平衡状态,一定达到化学平衡状态的是Ⅲ,且该反应正反应为吸热反应,即
可能达平衡状态,一定达到化学平衡状态的是Ⅲ,且该反应正反应为吸热反应,即![]() ,以此解答。
,以此解答。
A.该反应的![]() ,故 A正确;
,故 A正确;
B.假如容器Ⅲ中CO的体积分数为![]() ,根据
,根据
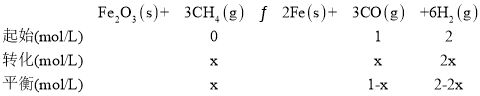
则![]() ,
,![]() ,故B错误;
,故B错误;
C.反应物和生成物都有固体,当容器中固体的质量不再改变,能说明反应已达平衡状态,故C错误;
D.根据以上分析,反应进行到![]() 时,三个容器中一定达到平衡状态的是Ⅲ ,故D错误。
时,三个容器中一定达到平衡状态的是Ⅲ ,故D错误。
故选:A。

【题目】下列实验中,对应的现象以及结论均正确的是( )
选项 | 实验操作 | 实验现象 | 结论 |
A | 取少量Na2SO3固体于试管中,加水溶解,滴加Ba(NO3)2溶液,再滴加稀硝酸 | 滴加Ba(NO3)2溶液,产生白色沉淀,再滴加稀硝酸,沉淀不溶解 | Na2SO3固体已经变质 |
B | 将SO2通入酸性KMnO4溶液中 | 溶液的紫红色褪去 | SO2具有漂白性 |
C | 将铁片投入浓硫酸中 | 无明显变化 | 常温下铁不与浓硫酸反应 |
D | 将10mL2mol/L的KI溶液与1mL1mol/LFeCl3溶液混合充分反应后滴加KSCN溶液 | 溶液颜色变红 | KI与FeCl3的反应具有可逆性 |
A.AB.BC.CD.D