题目内容
【题目】一定条件下,化学反应2H2+O2═2H2O的能量变化如图所示,则反应的热化学方程式可表示为( ) 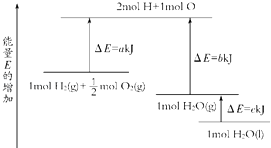
A.H2(g)+ ![]() ?O2(g)═H2O(g)△H=(a+b) kJ?mol﹣1
?O2(g)═H2O(g)△H=(a+b) kJ?mol﹣1
B.2H2(g)+O2(g)═2H2O(g)△H=2(b﹣a) kJ?mol﹣1
C.H2(g)+ ![]() ?O2(g)═H2O(l)△H=(b+c﹣a) kJ?mol﹣1
?O2(g)═H2O(l)△H=(b+c﹣a) kJ?mol﹣1
D.2H2(g)+O2(g)═2H2O(l)△H=2(a﹣b﹣c) kJ?mol﹣1
【答案】D
【解析】解:由图中分析判断,1molH2(g)+ ![]() molO2(g)的能量为aKJ,1molH2O(g)的能量为bKJ,所以H2(g)+
molO2(g)的能量为aKJ,1molH2O(g)的能量为bKJ,所以H2(g)+ ![]() O2(g)═H2O(g)△H=(a﹣b) kJmol﹣1 , 1molH2O(g)转化为1molH2O(l)放热为cKJ,所以得到:H2(g)+
O2(g)═H2O(g)△H=(a﹣b) kJmol﹣1 , 1molH2O(g)转化为1molH2O(l)放热为cKJ,所以得到:H2(g)+ ![]() O2(g)═H2O(l)△H=(a﹣b﹣c) kJmol﹣1;
O2(g)═H2O(l)△H=(a﹣b﹣c) kJmol﹣1;
即2H2(g)+O2(g)═2H2O(l)△H=2(a﹣b﹣c) kJmol﹣1 ,
故选D.
【考点精析】解答此题的关键在于理解反应热和焓变的相关知识,掌握在化学反应中放出或吸收的热量,通常叫反应热.

练习册系列答案
相关题目