题目内容
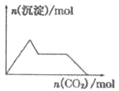
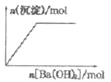
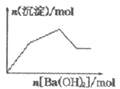
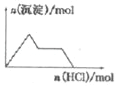
【题目】某100mL溶液中含有的部分离子浓度大小如图所示,该溶液可能还含有Fe3+、Ba2+、H+、SO42-、CO32-。为了进一步确认,对该溶液进行实验检测:

实验操作与现象 | 实验结论 | 判断理由 | |
步骤一 | 仔细观察坐标图 | 肯定无________。 | 肯定无该离子的理由______________。 |
步骤二 | 该溶液呈无色、透明、均一状态; | 肯定无________。 | 肯定无该离子的理由______________。 |
(1)实验操作的步骤三中称量沉淀前的实验操作步骤有:过滤、 _________、干燥、在干燥器中冷却。
(2)原溶液中H+物质的量浓度为 __________mol/L。
(3)向溶液中加入NaHCO3溶液,反应的离子方程式为:____________________________。
(4)若向 100mL 该溶液中加入 1mol/L 的 Ba(OH)2溶液,当Mg2+恰好沉淀完全时加入的Ba(OH)2溶液体积为_______L。
【答案】 CO32- 若有CO32-会与Mg2+生成微溶物 Fe3+ Fe3+棕黄色 电中性原则 洗涤 3mol/L HCO3 - +H+ = CO2 +H2O 0.2
【解析】溶液中含有镁离子,所以一定不含CO32-,该溶液呈无色、透明、均一状态,一定不含Fe3+,加入足量BaCl2溶液,生成23.3g即0.1mol白色沉淀硫酸钡,再加稀硝酸,沉淀不消失,一定含有硫酸根0.1mol,一定不含钡离子,因此溶液中一定含有0.1molSO42﹣、0.05mol Mg2+,0.1mol Na+,0.3mol Cl-,根据电荷守恒,阳离子所带正电荷总和:0.1mol×1+0.05×2mol=0.2mol,阴离子负电荷总和0.3mol×1+0.1mol×2=0.5mol,所以一定含有氢离子,故答案为:CO32-;碳酸根离子和镁离子之间会反应;Fe3+;该离子为黄色;电荷守恒;
(1)实验操作的步骤三中称量沉淀前的实验操作步骤有:过滤、洗涤、灼烧、在干燥器中冷却,故答案为:洗涤;
(2)原溶液中H+物质的量浓度=![]() =3mol/L,故答案为:3;
=3mol/L,故答案为:3;
(3)溶液中含有氢离子,向溶液中加入NaHCO3溶液,反应的离子方程式为:H++HCO3-=H2O+CO2↑,故答案为:H++HCO3-=H2O+CO2↑;
(4)100mL 该溶液中含有0.1mol SO42﹣、0.05mol Mg2+,0.1mol Na+,0.3mol Cl-,0.3molH+,向该溶液中加入1mol/L 的 Ba(OH)2溶液,沉淀0.1mol SO42﹣需要0.1mol Ba2+;沉淀0.05mol Mg2+,需要先中和0.3molH+,共需要0.15mol+0.05mol=0.2molBa(OH)2,因此一共需要0.2molBa(OH)2,体积是![]() =0.2L,故答案为:0.2。
=0.2L,故答案为:0.2。

 寒假天地重庆出版社系列答案
寒假天地重庆出版社系列答案