题目内容
下列对于乙烯(CH2=CH2)分子结构的描述中正确的是 ( )
| A.有6个σ键、0个π键 |
| B.3个sp3杂化轨道形成σ键、1个sp3杂化轨道形成π键 |
| C.C-H之间是s轨道与sp2轨道形成的σ键,C与C之间是未参加杂化的2p轨道形成的σ键和π键 |
| D.C与C之间是sp2杂化轨道形成的一个σ键和未参加杂化的2p轨道形成的π键 |
D
解析试题分析:单键都是σ键,双键或三键中含有π键,据此可知,乙烯分子中含有5个σ键、1个π键,A错误;乙烯是平面型结构,碳原子是sp2杂化,杂化轨道只能形成σ键,所以选项BC都是错误,D正确,答案选D。
考点:考查乙烯的分子结构特点
点评:该题是基础性试题的考查,主要是考查学生对乙烯分子结构的熟悉了解程度,特别是杂化轨道类型的掌握情况,有利于调动学生的学习兴趣,激发学生的学习积极性。

练习册系列答案
相关题目
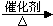 2CH3CHO+2H2O
2CH3CHO+2H2O +HO-NO2
+HO-NO2 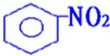 +H2O
+H2O