题目内容
在实验室中严禁打闹,某几个同学在做实验中打闹而同时把盛有浓盐酸和盛固体KClO3的试剂瓶打破,使其在地上混合立即产生大量黄绿色气体,发生反应的化学方程式为:
KClO3+ 6HCl(浓)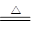 KCl+3Cl2↑ + 3 H2O
KCl+3Cl2↑ + 3 H2O
(1)该反应中的氧化剂是___________。
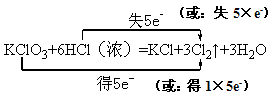
(2)在化学方程式上标出电子转移的方向和数目 。
(3)如反应中转移了0.50 mol电子,则产生的气体在标准状况下体积为________ L 。
(4)在清除碎片时某同学用湿毛巾捂住鼻子防止中毒,有以下四种溶液可浸湿毛巾,它们分别是:①NaOH溶液 ②NaCl溶液 ③KBr溶液 ④NaHCO3溶液. 正确选择是 (填试剂号数).
(2+2+2+2)
(1)KClO3
(2)
(3)6.72
(4) ④
解析(1) 该反应中的 KClO3中Cl由+5价降为0价,氧化剂是KClO3
(2)
(3)KClO3+6HCl=KCl+3Cl2+3H2O 5e―(转移电子数)
3×22.4lL 5mol
6.72L 0.50mol
(4) ④
其中①NaOH溶液强腐蚀性 ②NaCl溶液溶解的Cl2很少 ③KBr溶液产生Br2具有强氧化性腐蚀性。

练习册系列答案
 培优三好生系列答案
培优三好生系列答案 优化作业上海科技文献出版社系列答案
优化作业上海科技文献出版社系列答案
相关题目
 KCl+3Cl2↑ + 3 H2O
KCl+3Cl2↑ + 3 H2O KCl+3Cl2↑ + 3 H2O
KCl+3Cl2↑ + 3 H2O KCl+3Cl2↑
+ 3 H2O
KCl+3Cl2↑
+ 3 H2O