题目内容
下列表达方式错误的是( )
分析:A.二氧化碳是直线型分子;
B.路易斯结构式就是用短棍表示共价键,用小黑点表示非键合的孤电子对的结构式,也叫电子结构式;
C.sp3杂化道图是正四面体结构;
D.π键是原子间p电子肩并肩重叠形成的.
B.路易斯结构式就是用短棍表示共价键,用小黑点表示非键合的孤电子对的结构式,也叫电子结构式;
C.sp3杂化道图是正四面体结构;
D.π键是原子间p电子肩并肩重叠形成的.
解答:解:A.二氧化碳是直线型分子,该分子模型是V型分子模型示意图,故A错误;
B.路易斯结构式就是用短棍表示共价键,用小黑点表示非键合的孤电子对的结构式,也叫电子结构式,所以HClO的路易斯结构式为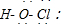 ,故B错误;
,故B错误;
C.一个s轨道和3个p轨道杂化,形成4个sp3杂化道,其空间构型是正四面体构型,故C正确;
D.π键是由两个原子的p电子肩并肩重叠形成的,所以其电子云图为: ,故D正确;
,故D正确;
故选AB.
B.路易斯结构式就是用短棍表示共价键,用小黑点表示非键合的孤电子对的结构式,也叫电子结构式,所以HClO的路易斯结构式为
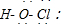 ,故B错误;
,故B错误;C.一个s轨道和3个p轨道杂化,形成4个sp3杂化道,其空间构型是正四面体构型,故C正确;
D.π键是由两个原子的p电子肩并肩重叠形成的,所以其电子云图为:
 ,故D正确;
,故D正确;故选AB.
点评:本题考查了化学用语,难度不大,注意π键的形成方式、路易斯结构式的书写.

练习册系列答案
相关题目
下列表达方式错误的是( )
A、二氧化碳的电子式是 | ||
B、氟化钠的电子式 | ||
C、S2-离子的结构示意图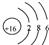 | ||
D、镁-24原子
|
下列表达方式错误的是( )
A、甲烷的电子式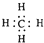 | ||
B、氟化钠的电子式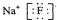 | ||
C、硫离子的结构示意图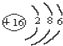 | ||
D、碳-12原子
|