题目内容
【题目】下表是周期表中的一部分,根据A-I在周期表中的位置,第(2) ~ (3)小题用元素符号或化学式回答,(4)~(6)小题按题目要求回答。
族 周期 | I A | Ⅱ A | Ⅲ A | Ⅳ A | Ⅴ A | Ⅵ A | Ⅶ A | O |
1 | A | |||||||
2 | D | E | G | |||||
3 | B | C | F | H | I |
(1)表中元素,化学性质最不活泼的原子结构示意图是___________,非金属性最强的元素在周期表中的位置是__________________________,
(2)最高价氧化物的水化物中碱性最强的是_________,酸性最强的是___________,
(3)A分别与D、E、G形成的最简单化合物中,最不稳定的_______________,
(4)A和E组成最简单化合物的电子______________
(5)在B、C、F、G的简单离子中,离子半径由大到小的顺序是__________________,
(6)由A的单质与O2构成的燃料电池中,在E的最高价氧化物对应水化物的条件下进行,写出正极的电极反应式______________________________________。
(7)当B的最高价氧化物的水化物与C的最高价氧化物反应后,向所得溶液中通入过量D的最高价氧化物的离子方程式___________________________________,
【答案】 第2周期第Ⅶ A族NaOHHClO4CH4
第2周期第Ⅶ A族NaOHHClO4CH4![]() S2—>F—>Na+>Al3+O2 + 4H+ + 4e-==2H2OAlO2— + 2H2O + CO2=Al(OH)3 ↓+ HCO3—
S2—>F—>Na+>Al3+O2 + 4H+ + 4e-==2H2OAlO2— + 2H2O + CO2=Al(OH)3 ↓+ HCO3—
【解析】
根据元素周期表的结构,表中A、B、C、D、E、F、G、H、I元素分别是H、Na、Al、C、N、P、F、Cl、Ar。(1)根据元素周期律可得化学性质最不活泼的应是惰性气体Ar,非金属性最强的元素为F,故答案为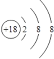 、第2周期第Ⅶ A族;(2)在表中所列元素中,金属性最强的是Na,最高价氧化物的水化物碱性最强的是NaOH;非金属性最强的是F,但是F无最高正价,则酸性最强的是应是HClO4,故答案为NaOH、H ClO4,(3)在D、E、G三种元素中非金属性最弱的为D,也是就碳元素,故它的氢化物最不稳定,故答案为CH4;(4)A和E组成的最简单的化合物为NH3,其电子式为
、第2周期第Ⅶ A族;(2)在表中所列元素中,金属性最强的是Na,最高价氧化物的水化物碱性最强的是NaOH;非金属性最强的是F,但是F无最高正价,则酸性最强的是应是HClO4,故答案为NaOH、H ClO4,(3)在D、E、G三种元素中非金属性最弱的为D,也是就碳元素,故它的氢化物最不稳定,故答案为CH4;(4)A和E组成的最简单的化合物为NH3,其电子式为![]() ;(5)B、C、F、G的简单离子分别为Na+、Al3+、S2—、F—,四种离子的最外层电子数相同,而硫离子比其余三种离子多一个电子层,半径最大,Na+、Al3+、F—三种离子的核外电子排布相同,核电荷数越大,半径反而越小,故半径的大小顺序为S2—>F—>Na+>Al3+;(6)在氢氧燃料电池中通入氧气的一极为正极,在酸性条件下的电极反应为O2 + 4H+ + 4e-==2H2O;(7)B的最高价氧化物的水化物与C的最高价氧化物反应后得到的是偏铝酸钠溶液,向其中通入过量的二氧化碳的离子方程式为AlO2— + 2H2O + CO2=Al(OH)3 ↓+ HCO3—,即得答案。
;(5)B、C、F、G的简单离子分别为Na+、Al3+、S2—、F—,四种离子的最外层电子数相同,而硫离子比其余三种离子多一个电子层,半径最大,Na+、Al3+、F—三种离子的核外电子排布相同,核电荷数越大,半径反而越小,故半径的大小顺序为S2—>F—>Na+>Al3+;(6)在氢氧燃料电池中通入氧气的一极为正极,在酸性条件下的电极反应为O2 + 4H+ + 4e-==2H2O;(7)B的最高价氧化物的水化物与C的最高价氧化物反应后得到的是偏铝酸钠溶液,向其中通入过量的二氧化碳的离子方程式为AlO2— + 2H2O + CO2=Al(OH)3 ↓+ HCO3—,即得答案。

 智能训练练测考系列答案
智能训练练测考系列答案