题目内容
8.用NA表示阿伏加德罗常数,下列叙述正确的是( )| A. | 常温下,5.85gNaCl固体中含有NaCl分子数为0.1NA | |
| B. | 标准状况下,22.4L水所含的原子数为3NA | |
| C. | 标准状况下,4g氦气中所含的原子数为NA | |
| D. | 0.5mol•L-1NaCl溶液中Cl-的物质的量为0.5mol |
分析 A、氯化钠为离子晶体;
B、标况下水为液体;
C、氦气由氦原子构成;
D、溶液体积不明确.
解答 解:A、氯化钠为离子晶体,故无氯化钠分子,故A错误;
B、标况下水为液体,故不能根据水的体积来计算其物质的量和原子个数,故B错误;
C、氦气由氦原子构成,故4g氦气中含有的氦原子的物质的量为n=$\frac{4g}{4g/mol}$=1mol,个数为NA个,故C正确;
D、溶液体积不明确,故溶液中的氯离子的个数无法计算,故D错误.
故选C.
点评 本题考查了阿伏伽德罗常数的有关计算,掌握物质的量的计算公式和物质结构是解题关键,难度不大.

练习册系列答案
 千里马走向假期期末仿真试卷寒假系列答案
千里马走向假期期末仿真试卷寒假系列答案
相关题目
18.化学是研究物质的组成、结构、性质以及变化规律的科学.请同学们根据所给信息,回答化学问题.
(1)化学已渗透到人类生活的各个方面,下列说法正确的是B
A.二氧化氮具有还原性,因此可用于自来水的杀菌消毒
B.可以用Si2N4、Al2O3制作高温结构陶瓷制品
C.在入海口的钢铁闸门上装一定数量的铜块可防止闸门被腐蚀
D.使用四乙基铅作汽油抗爆震剂,可减少汽车尾气污染
(2)已知:
为了除去MgCl2晶体中的杂质Fe3+,先将混合物溶于水,再加入足量的Mg(OH)2,充分反应,过滤,结晶.离子方程式为2Fe3++3Mg(OH)2=3Mg2++2Fe(OH)3.
(3)盐酸肼(N2H4Cl2)是一种重要的化工原料,属于离子化合物,易溶于水,溶液呈酸性,水解原理与NH4Cl类似.
①写出盐酸肼第一步水解反应的离子方程式:N2H62++H2O═[N2H5•H2O]++H+.
②盐酸肼水溶液中离子浓度的排列顺序正确的是D(填字母).
A.c(N2${H}_{4}^{2+}$)>c(Cl-)>c(H+)>c(OH-)
B.c(N2${H}_{4}^{2+}$)>c([N2H3•H2O]+)+(H+)=c(Cl-)+c(OH-)
C.c(Cl-)>c([N2H3•H2O]+)>c(H+)>c(OH-)
D.c(Cl-)>c(N2${H}_{4}^{2+}$)>c(H+)>c(OH-)
(1)化学已渗透到人类生活的各个方面,下列说法正确的是B
A.二氧化氮具有还原性,因此可用于自来水的杀菌消毒
B.可以用Si2N4、Al2O3制作高温结构陶瓷制品
C.在入海口的钢铁闸门上装一定数量的铜块可防止闸门被腐蚀
D.使用四乙基铅作汽油抗爆震剂,可减少汽车尾气污染
(2)已知:
| 物质/25℃ | Fe(OH)2 | Fe(OH)3 | Mg(OH)2 |
| 溶解度/g | 1.5×10-4 | 3.0×10-3 | 9.0×10-1 |
(3)盐酸肼(N2H4Cl2)是一种重要的化工原料,属于离子化合物,易溶于水,溶液呈酸性,水解原理与NH4Cl类似.
①写出盐酸肼第一步水解反应的离子方程式:N2H62++H2O═[N2H5•H2O]++H+.
②盐酸肼水溶液中离子浓度的排列顺序正确的是D(填字母).
A.c(N2${H}_{4}^{2+}$)>c(Cl-)>c(H+)>c(OH-)
B.c(N2${H}_{4}^{2+}$)>c([N2H3•H2O]+)+(H+)=c(Cl-)+c(OH-)
C.c(Cl-)>c([N2H3•H2O]+)>c(H+)>c(OH-)
D.c(Cl-)>c(N2${H}_{4}^{2+}$)>c(H+)>c(OH-)
19.某溶液中只含有K+,Mg2+,NO3-,SO42-四种离子,已知前三种离子的个数比为3:2:1,则溶液中Mg2+和 SO42-的离子个数比为( )
| A. | 2:3 | B. | 1:4 | C. | 3:4 | D. | 3:2 |
16.下列事实中,能证明氯化钠是离子化合物的是( )
| A. | 氯化钠易溶于水 | B. | 氯化钠的水溶液能导电 | ||
| C. | 熔融状态下氯化钠能导电 | D. | 氯化钠不易分解 |
3.下列说法正确的是( )
| A. | 元素的单质可由氧化或还原含该元素的化合物来制得 | |
| B. | 反应中失去电子越多的金属单质,其还原性就越强 | |
| C. | 阳离子只能得到电子被还原,只能作氧化剂 | |
| D. | 有单质参加的反应一定是氧化还原反应 |
17.乙醇分子中不同的化学键如图所示,对乙醇在各种反应中应断裂的键说明不正确的是( )


| A. | 与金属钠作用时,键②断 | |
| B. | 和乙酸、浓硫酸共热时,键①断裂 | |
| C. | 在空气中燃烧时,键①②③④⑤全部断裂 | |
| D. | 在铜催化下和氧气反应时,键①和③断裂 |
18.已知:2XO${\;}_{4}^{-}$+10A-+16H+═2X2++5A2+8H2O;2M3++2B-═2M2++B2;B2+YO2+2H2O═2B${\;}^{_}$+YO${\;}_{4}^{2-}$+4H+;A2+2M2+═2M3++2A-由以上信息判断下列哪个反应不能发生( )
| A. | YO${\;}_{4}^{2-}$+2M2++4H+═YO2+2M3++2H2O | |
| B. | 5M2++XO${\;}_{4}^{-}$+8H+═5M3++X2++4H2O | |
| C. | 2XO${\;}_{4}^{-}$+10B-+16H+═2X2++5B2+8H2O | |
| D. | A2+2B-═B2+2A- |
 .
.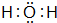 .
. .
.