题目内容
15.下列叙述错误的是( )| A. | 1mol任何物质都含有约6.02×1023个原子 | |
| B. | 0.012kg12C含有约6.02×1023个碳原子 | |
| C. | 物质的量是国际单位制中七个基本物理量之一 | |
| D. | 在使用摩尔表示物质的量的单位时,应指明粒子的种类 |
分析 物质的量是国际单位制中七个基本物理量之一,结合n=$\frac{m}{M}$=$\frac{N}{{N}_{A}}$,注意在使用摩尔表示物质的量的单位时,应指明粒子的种类,以此解答.
解答 解:A.分子不一定都单原子分子,如1mol氧气含有2mol原子,个数为12.04×1023,故A错误;
B.0.012kg12C为1mol,含有约6.02×1023个碳原子,故B正确;
C.物质的量是国际单位制中七个基本物理量之一,包括长度、质量、时间、电流、热力学温度、物质的量、发光强度等,故C正确;
D.物质的量是表示含有一定数目粒子的集合体,使用摩尔表示物质的量的单位时,应指明粒子的种类,故D正确.
故选A.
点评 本题考查物质的量的计算以及概念的理解,为高频考点,侧重于双基的考查,注意相关基础知识的积累,难度不大.

练习册系列答案
 百年学典课时学练测系列答案
百年学典课时学练测系列答案
相关题目
5.下列物质中属于电解质的是( )
①氢氧化钠 ②硫酸钡 ③铜 ④蔗糖 ⑤二氧化硫.
①氢氧化钠 ②硫酸钡 ③铜 ④蔗糖 ⑤二氧化硫.
| A. | ①② | B. | ①②⑤ | C. | ③④ | D. | ①⑤ |
6.下列与处理方法对应的反应方程式不正确的是( )
| A. | 工业上用水吸收NO2生产硝酸:3NO2+H2O═2HNO3+NO | |
| B. | 用氨水除去工业原料氯化铵中的氯化铁杂质:Fe3++3OH-═Fe(OH)3↓ | |
| C. | 用熟石灰处理泄漏的液氯:2Ca(OH)2+2Cl2═CaCl2+Ca(ClO)2+2H2O | |
| D. | 用明矾除去水中的悬浮颗粒物:Al3++3H2O?Al(OH)3 (胶体)+3H+ |
10.下列实验操作中正确的是( )
| A. | 应使混合物中的水分完全蒸干后,才能停止加热 | |
| B. | 分液操作时,下层液体从分液漏斗下口放出后再将上层液体从下口放出到另一个烧杯中 | |
| C. | 萃取操作时,应选择有机萃取剂,且萃取剂的密度必须比水大 | |
| D. | 蒸馏操作时,应使温度计水银球靠近蒸馏烧瓶的支管口处 |
20. 恒温密闭容器发生可逆反应:Z(?)+W(?)?X(g)+Y(?);△H,在t1时刻反应达到平衡,在t2时刻缩小容器体积,t3时刻再次达到平衡状态后未再改变条件.下列有关说法中正确的是( )
恒温密闭容器发生可逆反应:Z(?)+W(?)?X(g)+Y(?);△H,在t1时刻反应达到平衡,在t2时刻缩小容器体积,t3时刻再次达到平衡状态后未再改变条件.下列有关说法中正确的是( )
 恒温密闭容器发生可逆反应:Z(?)+W(?)?X(g)+Y(?);△H,在t1时刻反应达到平衡,在t2时刻缩小容器体积,t3时刻再次达到平衡状态后未再改变条件.下列有关说法中正确的是( )
恒温密闭容器发生可逆反应:Z(?)+W(?)?X(g)+Y(?);△H,在t1时刻反应达到平衡,在t2时刻缩小容器体积,t3时刻再次达到平衡状态后未再改变条件.下列有关说法中正确的是( )| A. | t1~t2时间段与t3时刻后,两时间段反应体系中气体的平均摩尔质量不可能相等 | |
| B. | Z和W在该条件下都不为气态 | |
| C. | 若在该温度下此反应平衡常数表达式为K=c(X),则t1~t2时间段与t3时刻后的X浓度不相等 | |
| D. | 若该反应只在某温度T0以上才能进行,则该反应的平衡常数K随温度升高而减小 |
7.价电子排布式为5s25p3的元素是( )
| A. | 第五周期第ⅢA族 | B. | 51号元素 | C. | sp区的主族元素 | D. | Te |
5.用如图所示的方法研究某气体的性质,这种方法是( )


| A. | 实验法 | B. | 观察法 | C. | 比较法 | D. | 分类法 |
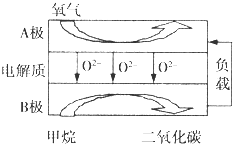 甲烷是天然气的主要成分,是生产生活中应用非常广泛的一种化学物质.
甲烷是天然气的主要成分,是生产生活中应用非常广泛的一种化学物质.