题目内容
糕点包装中常见的脱氧剂组成为还原性铁粉、氯化钠、炭粉等,其脱氧原理与钢铁的吸
氧腐蚀相同。下列分析正确的是
| A.含有 1.12g铁粉的脱氧剂,理论上最多能吸收氧气336mL(标准状况) |
| B.脱氧过程是吸热反应,可降低温度,延长糕点保质期 |
| C.脱氧过程中碳做原电池负极,电极反应为:2H2O+O2+4e-=4OH- |
| D.脱氧过程中铁作原电池正极,电极反应为:Fe-3e-=Fe3+ |
A
解析试题分析:A、1.12g铁粉的物质的量是0.2摩尔,脱氧原理中最终转化为三价铁,失去电子0.6摩尔,根据电子守恒,最多吸收氧气0.15摩尔,也就是336mL,正确;B、脱氧过程是放热反应,错误;C、碳作正极,错误;D、铁作负极,电极反应为:Fe-2e-=Fe2+,错误。
考点:考查吸氧腐蚀和物质的量计算

练习册系列答案
相关题目
用如图所示装置制取纯净的Fe(OH)2,下列说法不正确的是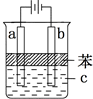
| A.a电极一定是铁,电解液c可以是CuCl2溶液 |
| B.电解一段时间,b电极附近pH升高 |
| C.溶液中的阴离子向a电极移动 |
| D.在加入苯之前应将电解液c加热煮沸 |
用铂电极电解某金属的氯化物(MCl2)溶液,当阳极上收集到1.12 L Cl2时(标准状况),阴极增重3. 2g.下列有关叙述正确的是
| A.M的相对原子质量为32 |
| B.电解过程中溶液的pH不发生变化 |
| C.M的相对原子质量为64 |
| D.电路中通过0.5mol电子 |
下列实验装置图合理的是 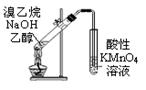
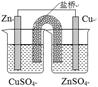
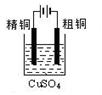
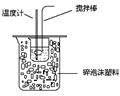
① ② ③ ④
| A.装置①可用于证明溴乙烷、NaOH、乙醇溶液共热生成乙烯 |
| B.装置②能构成锌铜原电池 |
| C.装置③可用于粗铜的电解精炼 |
| D.装置④可用于在实验室测定中和反应的反应热 |
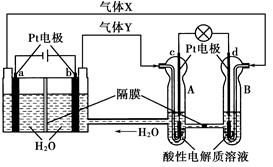
海水淡化的方法有多种,如蒸馏法、电渗析法等。电渗析法是一种利用离子交换膜进行离子交换的方法,其原理如图所示。已知海水中含Na+、Cl-、Ca2+、Mg2+、SO等离子,电极为惰性电极。下列叙述中正确的是( )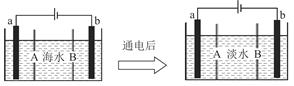
| A.B膜是阴离子交换膜 |
| B.通电后,海水中阳离子向a电极处运动 |
| C.通电后,a电极的电极反应式为4OH--4e-=O2↑+2H2↑ |
| D.通电后,b电极上产生无色气体,溶液中出现少量白色沉淀 |
研究人员研制出一种锂水电池,可作为鱼雷和潜艇的储备电源。电池以金属锂和钢板为电极材料,LiOH为电解质,使用时加入水即可放电。关于该电池的说法正确的是( )
| A.钢板为正极,发生还原反应 |
| B.放电时电子的流向:正极→导线→负极 |
| C.放电时OH-向正极移动 |
D.总反应为:2Li+2H+ 2Li++H2↑ 2Li++H2↑ |
下列与金属腐蚀有关的说法,正确的是( )。
| A.图1中,插入海水中的铁棒,越靠近底端腐蚀越严重 |
| B.图2中,往烧杯中滴加几滴KSCN溶液,溶液变血红色 |
| C.图3中,燃气灶的中心部位容易生锈,主要是由于高温下铁发生化学腐蚀 |
| D.图4中,用牺牲镁块的方法来防止地下钢铁管道的腐蚀,镁块相当于原电池的正极 |
某研究性学习小组用如图装置研究不同能量之间的转化问题。下列说法正确的是( )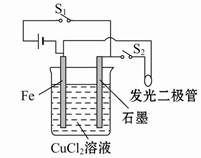
| A.断开开关S1,闭合开关S2,化学能转化为电能,电能转化为光能等 |
| B.断开开关S1,闭合开关S2,此时构成的装置属于电解池 |
| C.断开开关S2,闭合开关S1,此时构成的装置属于原电池 |
| D.断开开关S2,闭合开关S1,化学能转化为电能 |