题目内容
如图,将2 mL浓度为6 mol/L的盐酸用注射器通过橡皮塞慢慢注入,玻璃管中出现小气泡,气泡在溶液中逐渐上升的过程中消失。对该反应过程的推断不合理的是:
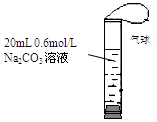

| A.有反应CO32- + 2H+ → CO2↑ + H2O发生 |
| B.有反应CO32- + H+ → HCO3-发生 |
| C.有反应CO32- + CO2 + H2O→ 2HCO3-发生 |
| D.加快盐酸注入速度不会改变反应现象 |
D
试题分析:由于是慢慢注入盐酸,反应的实质是CO32- + CO2 + H2O→ 2HCO3-,然后HCO3- + H+ → CO2↑ + H2O发生,但如果盐酸浓度局部过大时就很快会发生两个反应看到现象是有气泡产生,故ABC都有可能发生。

练习册系列答案
 举一反三同步巧讲精练系列答案
举一反三同步巧讲精练系列答案 口算与应用题卡系列答案
口算与应用题卡系列答案
相关题目
 Fe3+
Fe3+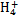
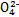 +H2O
+H2O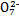 +H2O
+H2O 2Cr
2Cr Fe(SCN)2+ K1="200" ②Fe(SCN)2++SCN-
Fe(SCN)2+ K1="200" ②Fe(SCN)2++SCN- Fe(OH)3↓+3H+
Fe(OH)3↓+3H+ 2H++ SO3
2H++ SO3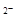
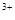 +3NH3·H2O= Al(OH)3↓+3NH4+
+3NH3·H2O= Al(OH)3↓+3NH4+