题目内容
标准状况下丙烷和某气态烯烃的混合物2.24L,经充分燃烧爆炸后,将生成的气体通过盛有足量NaOH溶液的烧杯中,得到碳酸钠固体的质量26.5g,求混合气体的成分和体积各是多少
碳酸钠固体的质量是26.5g
所以CO2的物质的量是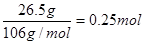
丙烷和烯烃的物质的量是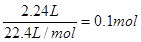
即含有的碳原子数的平均值是2.5
又因为最简单的烯烃是乙烯含有2个碳原子
所以混合气中必须含有乙烯
设乙烯和丙烷的物质的量分别是x和y,则
X+y=0.1mol、2x+3y=0.25
解得x=0.05mol、y=0.05mol
所以其体积都是0.05mol×22.4L/mol=1.12L
所以CO2的物质的量是
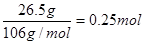
丙烷和烯烃的物质的量是
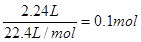
即含有的碳原子数的平均值是2.5
又因为最简单的烯烃是乙烯含有2个碳原子
所以混合气中必须含有乙烯
设乙烯和丙烷的物质的量分别是x和y,则
X+y=0.1mol、2x+3y=0.25
解得x=0.05mol、y=0.05mol
所以其体积都是0.05mol×22.4L/mol=1.12L
考查有机物燃烧的有关计算。

练习册系列答案
相关题目
 ________
________ 
 ③石炭酸 ④硬脂酸甘油酯
③石炭酸 ④硬脂酸甘油酯