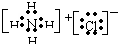题目内容
由短周期构成的离子化合物中,一个阳离子和一个阴离子的核外电子数之和为20,下列说法中正确的是 )
分析:由短周期元素构成的某离子化合物中,一个阳离子和一个阴离子核外电子数之和为20.阴、阳离子均是10电子微粒,它们可以是:阴离子:N3-、O2-、F-、OH-等,阳离子:NH4+、Na+、Mg2+、Al3+等,据此判断.
解答:解:由题意知阴、阳离子均是10电子微粒,它们可以是:阴离子:N3-、O2-、F-、OH-等,阳离子:NH4+、Na+、Mg2+、Al3+等.
A、对简单的离子,阴、阳离子电子层结构相同,核电荷数越大,离子半径越小,阳离子的核电荷数一定大于阴离子的核电荷数,所以该化合物中阳离子半径小于阴离子半径,故A错误;
B、离子化合物,一定有离子键,也可能含共价键,如NaOH、Mg(OH)2、NH4F等,故B错误
C、NH4+中氢元素在第一周期,所以构成该离子化合物的元素可能在第一周期,故C错误;
D、当阴、阳离子所电荷不相等,阳离子和阴离子个数不相等,如、MgF2、Na2O,当阴、阳离子所电荷相等,阳离子和阴离子个数相等,如NaF、NaOH,故D正确;
故选D.
A、对简单的离子,阴、阳离子电子层结构相同,核电荷数越大,离子半径越小,阳离子的核电荷数一定大于阴离子的核电荷数,所以该化合物中阳离子半径小于阴离子半径,故A错误;
B、离子化合物,一定有离子键,也可能含共价键,如NaOH、Mg(OH)2、NH4F等,故B错误
C、NH4+中氢元素在第一周期,所以构成该离子化合物的元素可能在第一周期,故C错误;
D、当阴、阳离子所电荷不相等,阳离子和阴离子个数不相等,如、MgF2、Na2O,当阴、阳离子所电荷相等,阳离子和阴离子个数相等,如NaF、NaOH,故D正确;
故选D.
点评:考查离子结构、物质结构等知识,难度中等,本题采取列举法解答,找出例外举例.列举法在元素周期表中经常利用.

练习册系列答案
 各地期末复习特训卷系列答案
各地期末复习特训卷系列答案 小博士期末闯关100分系列答案
小博士期末闯关100分系列答案
相关题目