题目内容
【题目】25°C时,用2a molL﹣1NaOH溶液滴定1.0L2a molL﹣1氢氟酸溶液,得到混合液中HF、F一的物质的量与溶液pH的变化关系如图所示.下列说法正确的是 ( )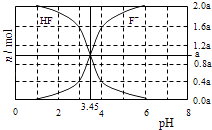
A.pH=3时,溶液中:c(Na+)<c(F一)
B.c(F一)>c(HF)时,溶液一定呈碱性
C.pH=4时,溶液中:c(HF)+c(Na+)+c(H+)﹣c(OH﹣)<2amolL﹣1
D.pH=3.45时,NaOH溶液恰好与HF完全反应
【答案】AC
【解析】解:A.pH=3时,c(H+)>c(OH﹣),溶液中存在c(Na+)+c(H+)=c(OH﹣)+c(F﹣),则c(F﹣)>c(Na+),故A正确; B.当pH>3.45时,c(F﹣)>c(HF),溶液可能呈酸性、中性或碱性,故B错误;
C.当pH=4时,混合溶液体积大于1.0L,c(F﹣)<1.6amol/L,c(HF)<0.4amol/L,溶液中存在c(Na+)+c(H+)=c(OH﹣)+c(F﹣),c(F﹣)=c(Na+)+c(H+)﹣c(OH﹣)<1.6amol/L,则c(HF)+c(Na+)+c(H+)﹣c(OH﹣)<2amolL﹣1 , 故C正确;
D.HF为弱酸,恰好反应时溶液应成碱性,当pH=3.45时HF酸过量,故D错误.
故选AC.

练习册系列答案
相关题目