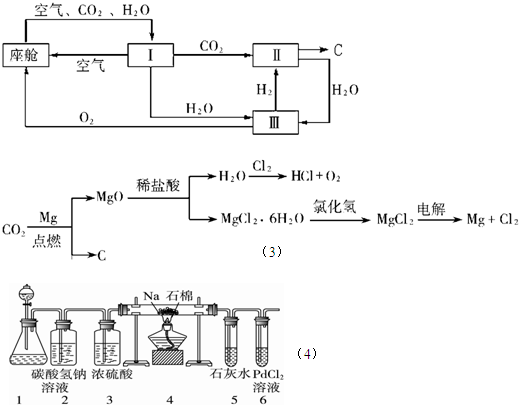
��Ŀ����
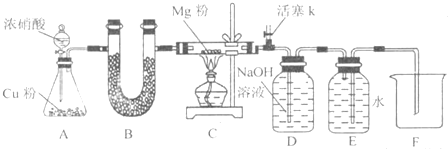
����Mg����CO2��ȼ�գ�ij��ȤС���Ʋ�NaӦ��Ҳ����CO2��ȼ�գ��ҹ���������ΪC��Na2O��Na2CO3�е����ֻ����֡���С��������ͼװ�ý�����ʵ��̽������֪PdCl2�ܱ�CO��ԭ�õ���ɫ��Pd��

�ش��������⣺
��1��Ϊ��ʹ��Ӧ�濪���ã������ͣ����ͼ���߷�����Ӧѡ�� װ��(����ͼ��ĸ����)����μ�����ѡװ�õ������� ��

��2��װ��2����ʢ�Լ�Ϊ ��
A��NaOH��Һ B������NaHCO3��Һ
C������Na2CO3��Һ D������NaCl��Һ
��3�����װ�õ���������ò�װ��ҩƷ���ڵ�ȼ�ƾ���ǰӦ�Ƚ���װ��1�еķ�Ӧ���������۲쵽 ����ʱ���ٵ�ȼ�ƾ��ƣ��ⲽ������Ŀ���� ��
��4����ʵ������ͽ�һ����̽���ó���Ӧ������
A��װ��6���к�ɫ�������ɣ�
B��ȡ��Ӧ��ֱ�����еĹ�������23.0g����������ˮ�У������ݲ����ҵõ��������Һ������Һ��ˮϡ�����250 mL����Һ��
C��ȡ25.00ml����B����Һ���μ�����BaCl2��Һ�������ɵİ�ɫ�������ˡ�ϴ�ӡ���������ù�������Ϊ1.97g��
�ٲ���C�в��������ǰ���뾭��ϴ�ӣ���μ���ó����Ƿ�ϴ�Ӹɾ� ��
�ڸ�̽���ó����������̼��Ӧ�Ļ�ѧ����ʽΪ ��
��1��C��2�֣����رյ��ɼУ���©���м�ˮ��һ��ʱ�����Һ�汣�ֲ�����˵�����������ã�2�֣�
��2��B��2�֣�
��3��װ��5�г��ִ������ǣ�2�֣����ž�װ���еĿ�����2�֣�
��4����ȡ���һ��ϴ��Һ����ϡH2SO4�������ֻ���˵������ϴ�Ӹɾ���2�֣�
��6Na+4CO2 2Na2O+Na2CO3+3CO��2�֣�
2Na2O+Na2CO3+3CO��2�֣�
��������
���������Cװ���Dz��ù�Һ�ֿ�����ƣ����ɼ�Һ����뷴Ӧ��ʼ���رյ��ɼз�Ӧ���������ѹǿʹ��Һ�ֿ���Ӧֹͣ�������ж�����ڵ�ʵ��װ�õ������ԣ�һ��ֻ����һ����ס�������ڽ���ʵ�飬�رյ��ɼУ���©���м�ˮ��һ��ʱ�����Һ�汣�ֲ�����˵�����������ã���2��װ��C����ʯ��ʯ�����ʯ�����ᷴӦ����������̼�������HCl���ʣ���2�ñ���NaHCO3��Һ����ȥHClͬʱת��Ϊ������̼����3��CO��ȼ�����п������ܻᷢ����ը����Ӧǰ����ͬ������̼��ȥװ���еĿ��������۲쵽5��ʯ��ˮ�����ʱ��Ϊװ���г���������̼�������ž�����4������ϴ���Ƿ�ɾ���һ����Ҫȡ���ε�ϴ��Һ�����м�����ܴ��ڵ��������ӣ�����ϴ��Һ������Ũ�Ƚϵͣ�һ�����Ƚ����׳����������������������ӡ������ӵȣ�
����ʵ������֪������̼���ʣ�����ʣ�࣬����̼�ᱵ�����������
n(Na2CO3)= n(BaCO3)=1.97��197��10=0.1mol
m(Na2CO3)= 0.1��106=10.6g
���Թ����к���������n(Na2O)=��23.0��10.6����62=0.2mol
����������ԭ��Ӧԭ������Ӧ��̼Ԫ�ػ��ϼ��½�Ϊ+2��CO������ʽΪ
6Na+4CO2 2Na2O+Na2CO3+3CO
2Na2O+Na2CO3+3CO
���㣺�����ۺ�ʵ�������ʵ��Ʊ�������й����⡣