题目内容
设NA为阿伏加德罗常数的值。下列叙述错误的是( )
A.常温常压下,8.8g CO2和N2O混合气体中所含的电子数为4.4NA
B.5.6 g铁与500 mL 2 mol·L-1硝酸反应,转移的电子数为0.2NA
C.常温常压下,0.4 mol Na2O2与足量H2O反应,共生成0.2 mol O2,转移电子的数目为0.4NA
D. V La mol·L-1的氯化铁溶液中,若Fe3+的数目为6.02×1023,则Cl-的数目大于3×6.02×1023
【知识点】计算A1 B3H3
【答案解析】B解析: CO2和N2O互为等电子体,二者的相对分子质量相同,因此8.8g CO2和N2O混合气体中所含的电子数为8.8×22/44=4.4mol,A正确;5.6g铁的物质的量为:0.1mol,500mL,2mol•L-1硝酸溶液中含有硝酸的物质的量为:2mol/L×0.5mol=1mol,硝酸过量,则0.1mol铁完全反应生成0.1mol铁离子,失去0.3mol电子,转移的电子数为0.3NA,B错误;0.4 mol Na2O2与足量H2O反应,共生成0.2 mol O2,转移电子的数目为0.2×2×(1-0)=0.4mol,C正确;D、若Fe3+没有水解,则Cl-的数目为Fe3+的3倍,但Fe3+会水解,使其个数比Cl-的1/3少,正确。
【思路点拨】解关于阿伏加德罗常数的试题需注意:氧化还原反应中电子转移(得失)数目方面的陷阱如本题的B、C项;考查电解质溶液中微粒数目或弱电解质的电离,盐类水解方面的知识;胶粒是许多分子的集合体,如1 mol铁完全转化为氢氧化铁胶体后,胶粒数远小于NA等。

.下表各选项中,不能利用置换反应通过Y得到W的一组化合物是( )
| 选项化合物 | A | B | C | D |
| Y | CO2 | Fe2O3 | SiO2 | FeCl3 |
| W | MgO | Al2O3 | CO | CuCl2 |


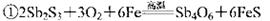
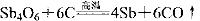 关于反应①、②的说法不正确的是
关于反应①、②的说法不正确的是