题目内容
20世纪50年代科学家提出价层电子对互斥模型(简称VSEPR模型),用于预测简单分子立体结构.其要点可以概括为:
Ⅰ、用AXnEm表示只含一个中心原子的分子组成,A为中心原子,X为与中心原子相结合的原子,E为中心原子最外层未参与成键的电子对(称为孤对电子),(n+m)称为价层电子对数.分子中的价层电子对总是互相排斥,均匀的分布在中心原子周围的空间;
Ⅱ、分子的立体构型是指分子中的原子在空间的排布,不包括中心原子未成键的孤对电子;
Ⅲ、分子中价层电子对之间的斥力主要顺序为:i、孤对电子之间的斥力>孤对电子对与共用电子对之间的斥力>共用电子对之间的斥力; ii、双键与双键之间的斥力>双键与单键之间的斥力>单键与单键之间的斥力; iii、X原子得电子能力越弱,A-X形成的共用电子对之间的斥力越强; iv、其他.
请仔细阅读上述材料,回答下列问题:
(1)根据要点I可以画出AXnEm的VSEPR理想模型,请填写下表:
(2)请用VSEPR模型解释CO2为直线型分子的原因
(3)H2O分子的立体构型为:
(4)SO2Cl2和SO2F2都属AX4E0型分子,S=O之间以双键结合,S-Cl、S-F之间以单键结合.请你预测 SO2Cl2和SO2F2分子的立体构型:
Ⅰ、用AXnEm表示只含一个中心原子的分子组成,A为中心原子,X为与中心原子相结合的原子,E为中心原子最外层未参与成键的电子对(称为孤对电子),(n+m)称为价层电子对数.分子中的价层电子对总是互相排斥,均匀的分布在中心原子周围的空间;
Ⅱ、分子的立体构型是指分子中的原子在空间的排布,不包括中心原子未成键的孤对电子;
Ⅲ、分子中价层电子对之间的斥力主要顺序为:i、孤对电子之间的斥力>孤对电子对与共用电子对之间的斥力>共用电子对之间的斥力; ii、双键与双键之间的斥力>双键与单键之间的斥力>单键与单键之间的斥力; iii、X原子得电子能力越弱,A-X形成的共用电子对之间的斥力越强; iv、其他.
请仔细阅读上述材料,回答下列问题:
(1)根据要点I可以画出AXnEm的VSEPR理想模型,请填写下表:
| n+m | 2 | 4 4 |
| VSEPR理想模型 | 直线形 直线形 |
正四面体 |
| 价层电子对之间的理想键角 | 180° 180° |
109°28′ |
CO2属AX2E0,n+m=2,故CO2为直线形
CO2属AX2E0,n+m=2,故CO2为直线形
.(3)H2O分子的立体构型为:
V形
V形
,请你预测水分子中∠H-O-H的大小范围为<109°28′
<109°28′
,原因是水分子属AX2E2,n+m=4,VSEPR理想模型为正四面体,价层电子对之间的夹角均为109°28′.根据Ⅲ-i,应有∠H-O-H<109°28′
水分子属AX2E2,n+m=4,VSEPR理想模型为正四面体,价层电子对之间的夹角均为109°28′.根据Ⅲ-i,应有∠H-O-H<109°28′
.(4)SO2Cl2和SO2F2都属AX4E0型分子,S=O之间以双键结合,S-Cl、S-F之间以单键结合.请你预测 SO2Cl2和SO2F2分子的立体构型:
四面体
四面体
.分析:(1)当n+m=4时,VSEPR模型为四面体形,当n+m=2时,VSEPR模型为直线形;
(2)根据CO2属AX2E0,n+m=2,VSEPR模型为直线形;
(3)根据H2O属AX2E2,n+m=4,VSEPR模型为四面体形,但氧原子有2对孤电子对来判断分子的立体构型;水分子属AX2E2,n+m=4,VSEPR理想模型为正四面体,价层电子对之间的夹角均为109°28′,根据Ⅲ-i来判断键角;
(4)当n+m=4时,VSEPR模型为四面体形,硫原子无孤电子对来判断分子的立体构型.
(2)根据CO2属AX2E0,n+m=2,VSEPR模型为直线形;
(3)根据H2O属AX2E2,n+m=4,VSEPR模型为四面体形,但氧原子有2对孤电子对来判断分子的立体构型;水分子属AX2E2,n+m=4,VSEPR理想模型为正四面体,价层电子对之间的夹角均为109°28′,根据Ⅲ-i来判断键角;
(4)当n+m=4时,VSEPR模型为四面体形,硫原子无孤电子对来判断分子的立体构型.
解答:解:(1)当n+m=4时,VSEPR模型为四面体形,其键角是109°28′,当n+m=2时,VSEPR模型为直线形,其键角是180°,
故答案为:
(2)CO2属AX2E0,n+m=2,VSEPR模型为直线形,所以CO2为直线形;
故答案为:CO2属AX2E0,n+m=2,故CO2为直线形;
(3)H2O属AX2E2,n+m=4,VSEPR模型为四面体形,但氧原子有2对孤电子对,所以分子的构型为V形;
水分子属AX2E2,n+m=4,VSEPR理想模型为正四面体,价层电子对之间的夹角均为109°28′,根据Ⅲ-i,应有∠H-O-H<109°28′,
故答案为:<109°28;水分子属AX2E2,n+m=4,VSEPR理想模型为正四面体,价层电子对之间的夹角均为109°28′;
(4)当n+m=4时,VSEPR模型为四面体形,硫原子无孤电子对,所以分子构型为四面体,故答案为:四面体.
故答案为:
| n+m | 4 | |
| VSEPR理想模型 | 直线形 | |
| 价层电子对之间的理想键角 | 180° |
故答案为:CO2属AX2E0,n+m=2,故CO2为直线形;
(3)H2O属AX2E2,n+m=4,VSEPR模型为四面体形,但氧原子有2对孤电子对,所以分子的构型为V形;
水分子属AX2E2,n+m=4,VSEPR理想模型为正四面体,价层电子对之间的夹角均为109°28′,根据Ⅲ-i,应有∠H-O-H<109°28′,
故答案为:<109°28;水分子属AX2E2,n+m=4,VSEPR理想模型为正四面体,价层电子对之间的夹角均为109°28′;
(4)当n+m=4时,VSEPR模型为四面体形,硫原子无孤电子对,所以分子构型为四面体,故答案为:四面体.
点评:本题主要考查了价层电子对互斥模型判断分子的结构,难度不大,注意概念的把握.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
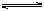 金刚石
金刚石  H>0.20世纪50年代,美国通用汽车公司在实验室利用高温高压(2000℃,20000atm)将石墨变成金刚石后,1989年,日本科学家用炸药和碳粉“炸出”金刚石的消息引起了人们广泛关注.它们将炸药和碳粉混合并用石蜡固化后装入钢制敞口容器内,沉入一个直径为8m、深约5m的混凝土水槽内,点火起爆,最后将容器里的水取出静置,可获得直径约为0.002
H>0.20世纪50年代,美国通用汽车公司在实验室利用高温高压(2000℃,20000atm)将石墨变成金刚石后,1989年,日本科学家用炸药和碳粉“炸出”金刚石的消息引起了人们广泛关注.它们将炸药和碳粉混合并用石蜡固化后装入钢制敞口容器内,沉入一个直径为8m、深约5m的混凝土水槽内,点火起爆,最后将容器里的水取出静置,可获得直径约为0.002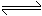 金刚石-Q(该反应吸热).20世纪50年代,美国通用汽车公司在实验室利用高温、高压(2000℃、20000atm)将石墨转化成金刚石之后,1989年,日本科学家用炸药和炭粉“炸出”金刚石的消息引起了人们的广泛关注.他们将炸药和炭粉混合并用石蜡固化后装入钢制敞口容器,沉入一个直径9m深约5m的混凝土水槽内,点火起爆,最后将容器里的水取出静置,可获得直径为0.002~0.003pm的超细金刚石粉.根据以上信息,回答问题.
金刚石-Q(该反应吸热).20世纪50年代,美国通用汽车公司在实验室利用高温、高压(2000℃、20000atm)将石墨转化成金刚石之后,1989年,日本科学家用炸药和炭粉“炸出”金刚石的消息引起了人们的广泛关注.他们将炸药和炭粉混合并用石蜡固化后装入钢制敞口容器,沉入一个直径9m深约5m的混凝土水槽内,点火起爆,最后将容器里的水取出静置,可获得直径为0.002~0.003pm的超细金刚石粉.根据以上信息,回答问题.