题目内容
已知AgNO3晶体加热分解生成两种单质和红棕色气体。用下列某些装置粗略测定混入了其他不分解也不参与反应的杂质的硝酸银的纯度,并进行有关实验(装置中必要的铁架台、铁夹、酒精灯等已略去),填写下列空白。
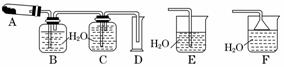
(1)写出AgNO3受热分解的化学方程式:___________________________________
________________________________________________________________________。
(2)测定AgNO3的纯度,可选用由A、B、C、D组成的装置,但其中不合理的是____________,该错误引起的后果是____________________________________________。
(3)B瓶中的空气对实验结果________(填“有”或“无”)影响,理由是______________
______________________________________________________________。
(4)如果改进装置后,称取硝酸银试样4.00 g置于A中缓缓加热,待反应完全后,产生的气体通过B、C装置后,测得量筒中水的体积,并折算成标准状况下气体的体积为112 mL,则试样的纯度为________。
(5)如果加热Cu(NO3)2生成氧化铜,则加热分解所得气体应通入装置________(填“E”或“F”),其理由是__________________________________________________________。
解析:(1)AgNO3晶体加热分解生成Ag、O2以及红棕色NO2气体。(2)测定AgNO3分解产生的气体的体积利用排水法测定,若气体从长导管进,无法将水排入量筒。(3)AgNO3分解产生的气体VNO2∶VO2=2∶1,4NO2+O2+H2O===4HNO3,O2过量,通入水后有O2剩余,B瓶中的空气对实验结果无影响。(4)根据AgNO3分解产生的气体VNO2∶VO2=2∶1和4NO2+O2+H2O===4HNO3以及剩余O2的物质的量为0.005 mol,可推知AgNO3分解产生的O2为0.01 mol。根据2AgNO3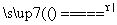 2Ag+2NO2↑+O2↑,可知AgNO3为3.4 g,则试样的纯度为85.0%。(5)根据2Cu(NO3)2
2Ag+2NO2↑+O2↑,可知AgNO3为3.4 g,则试样的纯度为85.0%。(5)根据2Cu(NO3)2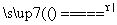 2CuO+4NO2↑+O2↑,分解产生的气体VNO2∶VO2=4∶1,恰好被水完全吸收,为防止液体倒吸而应选装置F。
2CuO+4NO2↑+O2↑,分解产生的气体VNO2∶VO2=4∶1,恰好被水完全吸收,为防止液体倒吸而应选装置F。
答案:(1)2AgNO3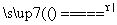 2Ag+2NO2↑+O2↑
2Ag+2NO2↑+O2↑
(2)C 无法将水排入量筒
(3)无 AgNO3分解产生的气体VNO2∶VO2=2∶1,通入水后有O2剩余
(4)85.0%
(5)F Cu(NO3)2分解产生的气体VNO2∶VO2=4∶1,恰好被水完全吸收,为防止液体倒吸而应选装置F

请回答下列问题:
(1)在一定温度下,下列叙述是可逆反应A(g)+3B(g) 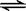 2C(g)达到平衡的标志的是
2C(g)达到平衡的标志的是
①C的生成速率与C的分解速率相等;
②单位时间生成amol A,同时生成3amol B;
③A、B 、C的浓度不再变化;
、C的浓度不再变化;
④A、B、C的分子数目比为1:3:2 ;
⑤混合气体的总压强不再变化;
⑥混合气体的物质的量不再变化;
⑦单位时间消耗amol A,同时生成3amol B;
⑧单位时间内生成a mol C,同时生成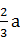 mol B
mol B
(2)在稀氨水中存在下述电离平衡NH3+H2O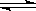 NH3 ·H2O
NH3 ·H2O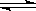 NH4++OH-,分别加入少量下列物质,溶液中c(OH-)如何变化?(填“增大”、“减小”或“不变”);平衡移动方向如何?(填“正向移动”或“逆向移动”)
NH4++OH-,分别加入少量下列物质,溶液中c(OH-)如何变化?(填“增大”、“减小”或“不变”);平衡移动方向如何?(填“正向移动”或“逆向移动”)
| 加入的物质 | 少量NH4Cl | 少量KOH溶液 |
| c(OH-)的变化 | ||
| 平衡移动方向 |
下述实验设计能够达到目的的是( )
| 编号 | 实验目的 | 实验设计 |
| A | 证明盐酸酸性比醋酸强 | 用同一电路测等体积的盐酸、醋酸溶液的导电性 |
| B | 证明H2CO3酸性比H2SiO3强 | 将CO2通入Na2SiO3溶液中 |
| C | 证明钠的金属活动性比铜强 | 向CuCl2溶液中投入金属钠 |
| D | 证明溶液中含有I- | 向溶液中加入淀粉 |
 。某研究性学习小组利用这种废液来制取较纯净的氯化钾晶体及液溴(Br2),设计了如下流程图:
。某研究性学习小组利用这种废液来制取较纯净的氯化钾晶体及液溴(Br2),设计了如下流程图: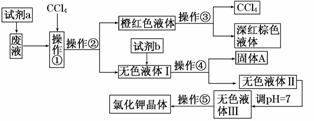

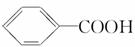 )和山梨酸(CH3CH == CH—CH == CH—COOH)都是常用食品防腐剂。下列关于这两种酸的叙述正确的是
)和山梨酸(CH3CH == CH—CH == CH—COOH)都是常用食品防腐剂。下列关于这两种酸的叙述正确的是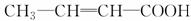 。现有下列说法,试根据巴豆酸的结构特点,判断在一定条件下,能与巴豆酸反应的物质是
。现有下列说法,试根据巴豆酸的结构特点,判断在一定条件下,能与巴豆酸反应的物质是