题目内容
(14分)W、X、Y、Z四种短周期元素在元素周期表中的位置如图所示,其中Z位于ⅦA族。请回答下列问题。

(1)W的原子结构示意图为 。能说明Z的非金属性比X的金属性强的事实是 (举一例)。
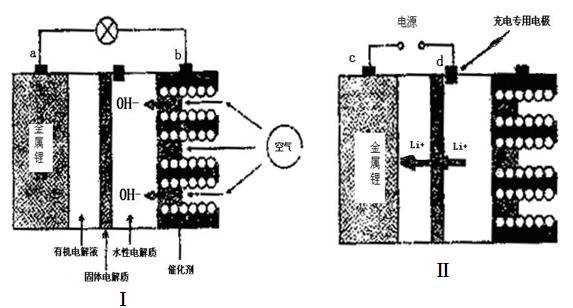
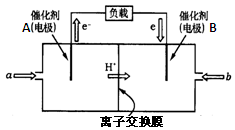
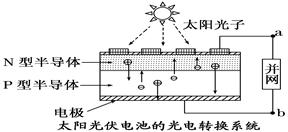
(2)W、Y和氢可形成原子个数比为1:1:4的化合物,工业酒精中含有此物质。该化合物的一个重要作用是用作燃料电池,如图是2004年批量生产的以该物质为燃料的燃料电池结构示意图。则a通入的物质为 ,B电极反应式为 。
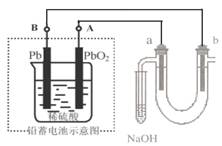
(3)电解NaZ水溶液时,阴极的电极反应式为 。工业上,用上述反应的阳极产物和Ca(OH)2为原料,制备漂白粉反应的化学方程式为 。
(4)已知:298K时,金属钠与Y2气体反应,生成1 mol Na2Y固体时,放出热量414 kJ;生成1 mol Na2Y2固体时,放出热量511 kJ。由Na2Y固体与Y2气体反应生成Na2Y2固体的热化学方程式为 。

(1)W的原子结构示意图为 。能说明Z的非金属性比X的金属性强的事实是 (举一例)。
(2)W、Y和氢可形成原子个数比为1:1:4的化合物,工业酒精中含有此物质。该化合物的一个重要作用是用作燃料电池,如图是2004年批量生产的以该物质为燃料的燃料电池结构示意图。则a通入的物质为 ,B电极反应式为 。

(3)电解NaZ水溶液时,阴极的电极反应式为 。工业上,用上述反应的阳极产物和Ca(OH)2为原料,制备漂白粉反应的化学方程式为 。
(4)已知:298K时,金属钠与Y2气体反应,生成1 mol Na2Y固体时,放出热量414 kJ;生成1 mol Na2Y2固体时,放出热量511 kJ。由Na2Y固体与Y2气体反应生成Na2Y2固体的热化学方程式为 。

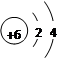 W―C、X―P、Y―O、Z―Cl
W―C、X―P、Y―O、Z―Cl⑴ 酸性:HClO4 >H3PO4 或氢化物的稳定性:HCl>PH3
⑵CH3OH,B为正极:O2+4H++4e―=2H2O
⑶电解NaCl水溶液:阴极的电极反应2H++2e―=H2↑;工业制漂白粉:2Cl2+2Ca(OH)2=CaCl2+Ca(ClO)2+2H2O;
⑷2Na(s)+1/2O2(g)=Na2O(s) △H=―414kJ/mol①
2Na(s)+O2(g)=NaO2(s) △H=―511kJ/mol②
②―①得:Na2O(s)+1/2O2(g)=Na2O2△H=―97kJ/mol

练习册系列答案
相关题目

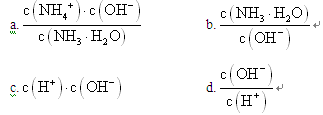
 原电池工作时电解质溶液中向正极移动的离子是_____________。
原电池工作时电解质溶液中向正极移动的离子是_____________。