题目内容
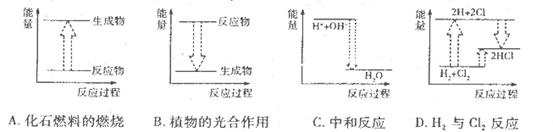
下列各反应的能量变化分别用如下形式的示意图表示,其中正确的是

C
试题分析:A、化石燃料的燃烧是放热反应,反应物的能量高于生成物,图象不符合,错误;B、植物光合作用是绿色植物把二氧化碳和水合成有机物,释放氧气,同时把光能转变成化学能储存在合成的有机物中的过程,过程中反应物能量低于生成物,错误;C、中和反应是放热反应,反应物总能量高于生成物总能量,正确;D、氢气与氯气的反应是放热反应,反应过程中拆化学键吸收能量,形成化学键放出能量,反应放出的能量高于吸收的能量,反应是放热反应,反应物能量应高于生成物,错误,答案选C。

练习册系列答案
 名校课堂系列答案
名校课堂系列答案
相关题目

 FeS
FeS 
 HCHO(g)+H2(g),甲醇的平衡转化率随温度变化曲线如下图所示。回答下列问题:
HCHO(g)+H2(g),甲醇的平衡转化率随温度变化曲线如下图所示。回答下列问题: