题目内容
【题目】锌和铝都是活泼金属,其氢氧化物既能溶于强酸,又能溶于强碱。但是氢氧化铝不溶于氨水,而氢氧化锌能溶于氨水,生成Zn(NH3)42+。回答下列问题:
(1)单质铝溶于氢氧化钠溶液的化学方程式:__________________________。
(2)锌和氢氧化钠溶液反应后,溶液中锌元素的存在形式为_________(用化学式表示)。
(3)下列各组中的两种溶液,用相互滴加的实验方法即可鉴别的是_______________。
① 硫酸铝和氢氧化钠 ② 硫酸锌和氢氧化钠 ③硫酸铝和氨水 ④ 硫酸锌和氨水
(4)在火箭和导弹技术中,将铝粉与石墨、TiO2按一定比例混合均匀,涂在金属表面,在高温下煅烧,金属表面生成TiC和另一种耐高温的物质,写出该反应的化学方程式:__________。
(5)某混合物![]() ,含有
,含有![]() 、
、![]() 和
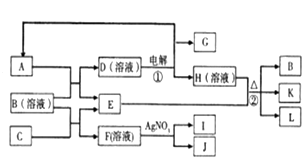
和![]() ,在一定条件下可实现如图所示的物质之间的变化:
,在一定条件下可实现如图所示的物质之间的变化:

据此回答下列问题:
①写出固体![]() 的化学式:
的化学式: ![]() __________;
__________;
②写出D与稀硫酸反应的化学方程式:___________________________________________;
写出反应①的离子方程式:_________________________________________。
【答案】 2Al+2NaOH+2H2O=2NaAlO2+3H2↑ Na2ZnO2 ①②④ 4Al+3C+3TiO2![]() 2Al2O3+3TiC Al2O3 Fe2O3+ 3H2SO4
2Al2O3+3TiC Al2O3 Fe2O3+ 3H2SO4![]() Fe 2(SO4) 3+ 3H2O Al2O3 + 2OH
Fe 2(SO4) 3+ 3H2O Al2O3 + 2OH ![]() 2AlO2+ H2O
2AlO2+ H2O
【解析】(1)单质铝与氢氧化钠溶液反应生成偏氯酸钠和氢气,反应的方程式为2Al+2NaOH+2H2O=2NaAlO2+3H2↑。(2)迁移铝与氢氧化钠溶液的反应写出锌和氢氧化钠溶液反应的化学方程式为Zn + 2NaOH=Na2ZnO2+H2↑,所以锌和氢氧化钠溶液反应后,溶液中锌元素的存在形式为Na2ZnO2。(3)① 将硫酸铝溶液逐滴加入氢氧化钠溶液至过量,一开始不产生沉淀,最终生成氢氧化铝沉淀;将氢氧化钠溶液逐滴加入硫酸铝溶液中先生成白色沉淀,氢氧化钠过量后氢氧化铝后消失。可以鉴别。②将硫酸锌溶液逐滴加入氢氧化钠溶液至过量,一开始不产生沉淀,最终生成氢氧化铝沉淀;将氢氧化钠溶液逐滴加入硫酸锌溶液中先生成白色沉淀,氢氧化钠过量后氢氧化锌后消失。可以鉴别。③硫酸铝和氨水,无论滴加顺序如何,均生成氢氧化铝白色沉淀,无法鉴别。④将硫酸锌溶液逐滴加入氨水中至过量,一开始不产生沉淀,最终生成氢氧化铝沉淀;将氨水逐滴加入硫酸锌溶液中先生成白色沉淀氢氧化锌后消失。可以鉴别。选①②④。(4)根据信息知铝粉与石墨、TiO2在高温下反应生成TiC和Al2O3,该反应的化学方程式为4Al+3C+3TiO2![]() 2Al2O3+3TiC。(5)将混合物A溶于水,过滤,溶液为硫酸铝钾溶液,固体C为氧化铁和氧化铝的混合物,加入氢氧化钠溶液,氧化铝和氢氧化钠溶液反应生成偏铝酸钠和水,固体D为氧化铁,向偏铝酸钠溶液中加入适量盐酸,二者发生反应生成氢氧化铝沉淀和氯化钠,氢氧化铝受热分解生成氧化铝和水,固体B为氧化铝;向硫酸铝钾溶液加入过量氨水,生成氢氧化铝沉淀和硫酸钾、硫酸铝的混合液,则①固体B为Al2O3;②D为氧化铁,氧化铁与稀硫酸反应生成硫酸铁和水,化学方程式为Fe2O3+ 3H2SO4=Fe 2(SO4) 3+ 3H2O;氧化铝和氢氧化钠溶液反应生成偏铝酸钠和水,离子方程式为Al2O3 + 2OH =2AlO2+ H2O。
2Al2O3+3TiC。(5)将混合物A溶于水,过滤,溶液为硫酸铝钾溶液,固体C为氧化铁和氧化铝的混合物,加入氢氧化钠溶液,氧化铝和氢氧化钠溶液反应生成偏铝酸钠和水,固体D为氧化铁,向偏铝酸钠溶液中加入适量盐酸,二者发生反应生成氢氧化铝沉淀和氯化钠,氢氧化铝受热分解生成氧化铝和水,固体B为氧化铝;向硫酸铝钾溶液加入过量氨水,生成氢氧化铝沉淀和硫酸钾、硫酸铝的混合液,则①固体B为Al2O3;②D为氧化铁,氧化铁与稀硫酸反应生成硫酸铁和水,化学方程式为Fe2O3+ 3H2SO4=Fe 2(SO4) 3+ 3H2O;氧化铝和氢氧化钠溶液反应生成偏铝酸钠和水,离子方程式为Al2O3 + 2OH =2AlO2+ H2O。

 阅读快车系列答案
阅读快车系列答案