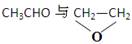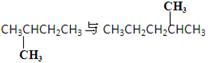题目内容
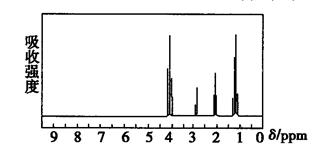
某有机物由C、H、O三种元素组成,将该有机物3g充分燃烧生成0.15mol二氧化碳和3.6g水,已知该有机物的蒸汽密度为2.68 g/L(折算成标准状况)。该有机物能与金属钠反应。则:
(1)通过计算求出该有机物的分子式为 ;
(2)写出该有机物的结构简式为 、 。
(3)取3g该有机物与金属钠反应,产生H2的体积为 (标况下)
(4)将该有机物与浓硫酸共热可制得烯烃,请写出反应方程式
(1)通过计算求出该有机物的分子式为 ;
(2)写出该有机物的结构简式为 、 。
(3)取3g该有机物与金属钠反应,产生H2的体积为 (标况下)
(4)将该有机物与浓硫酸共热可制得烯烃,请写出反应方程式

试题分析:(1)该有机物的蒸汽密度为2.68 g/L(折算成标准状况)
则该有机物的相对分子质量是2.68×22.4=60
则3g有机物的物质的量是0.05mol
生成水和CO2的物质的量分别是0.2mol和0.15mol
则根据原子守恒可知
有机物中碳氢原子的质量分别是0.15mol×12g/mol=1.8g、0.4g
所以根据质量守恒定律可知
有机物中氧原子的质量是3g-1.8g-0.4g=0.8g
则含有的氧原子的物质的量是0.05mol
所以该有机物中C、H、O三种原子的个数之比是3:8:1
由于碳原子已经达到饱和状态
乙醇该有机物的分子式就是C3H8O
(2)该有机物能与金属钠反应,则根据化学式可知,该有机物是醇类,表示醚类,所以结构简式是CH3CH2CH2OH或CH3CHOHCH3
(3)3g有机物的物质的量是0.05mol
则根据氢原子守恒可知
生成氢气的物质的量是0.05mol÷2=0.025mol
所以标准状况下氢气的体积是0.025mol×22.4/L=0.56L
(4)丙醇可以发生消去反应生成丙烯,则反应的化学方程式是CH3CH2CH2OH
 CH3CH=CH2↑+H2O或CH3CHOHCH3
CH3CH=CH2↑+H2O或CH3CHOHCH3 CH2=CHCH3↑+H2O。
CH2=CHCH3↑+H2O。点评:该题是中等难度的试题,试题基础性强,侧重能力的培养和训练。有助于培养学生的逻辑推理能力和发散思维能力,也有助于培养学生的规范答题能力,提高学生分析问题、解决问题的能力。

练习册系列答案
 黄冈创优卷系列答案
黄冈创优卷系列答案
相关题目