题目内容
NaH是离子化合物,与水反应可生成碱和氢气。现有NaH与Al粉混合物共mg,跟足量水反应共收集到氢气的质量为ng,则原混合物中Al粉的质量可能为
A.(12n-m)g B.(24m-5n)g C.(36n-3m)g D.(m-24n/5)g
CD
【解析】
试题分析:依题意,本题可分两种情况讨论,第一种情况NaH过量Al不足。设NaH xmol,Al ymol。
NaH + H2O = NaOH + H2↑ 2Al + 2NaOH = 2NaAlO2 + 3H2↑
xmol xmol ymol 1.5ymol
所以
24x+27y=m 解得 x=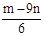 则Al的质量为27×
则Al的质量为27×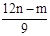 =(36n-3m)g。
=(36n-3m)g。
2x+3y=n y=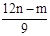
第二种情况NaH不足,Al过量,设NaH xmol,Al ymol
NaH + H2O = NaOH + H2↑ 2Al + 2NaOH = 2NaAlO2 + 3H2↑
xmol xmol xmol xmol 1.5xmol
则2x+3x=n,x=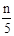 ,所以NaH的质量为(24n/5)g,Al的质量为(m-24n/5)g。
,所以NaH的质量为(24n/5)g,Al的质量为(m-24n/5)g。
答案选CD。
考点:化学计算
点评:本题难度较大,主要是要进行讨论,当Al过量时,氢气的量由NaOH的量决定。

氢元素与其他元素形成的二元化合物称为氢化物。下面关于氢化物的叙述正确( )
| A.D2O与H2O是同位素 | B.SiH4的稳定性>CH4的稳定性 |
| C.氢氟酸的酸性>盐酸的酸性 | D.NaH是离子化合物,其电子式为Na+[ xH] |