题目内容
四种主族元素的离子aXm+、bYn+、cZn-和dRm-(a、b、c、d为元素的原子序数),它们具有相同的电子层结构,若m>n,则对下列叙述的判断正确的是( )
①a-b=m-n
②元素的原子序数a>b>c>d
③元素非金属性Z>R
④最高价氧化物对应水化物的碱性X>Y
A.②③ B.③ C.①②③④ D.①②③
D
【解析】
试题分析:金属元素的原子失去电子变为阳离子,非金属元素的原子获得电子变为阴离子。原子失去或获得的电子越多,其所带的电荷就越多。根据题意可得:①a-m=b-n ,整理可得a-b=m-n。正确。由于这几种离子的电子层结构相同,Xm+、bYn+是阳离子,失去的电子m>n,所以原子序数a>b;cZn-和dRm-是阴离子,得到的电子m>n,所以原子序数c>d.。阳离子的原子序数大于阴离子的原子序数。所以元素的原子序数a>b>c>d.正确。③同一周期的元素,原子序数越大,元素非金属性越强,由于Z的原子序数大于R的原子序数,所以非金属性Z>R。正确。④同一周期的元素,原子序数越大,元素的金属性就越弱。原子序数X>Y。所以最是高价氧化物对应水化物的碱性Y>X。错误。
考点:考查电子层结构相同的微粒的原子序数、元素的电子及化合物的性质的知识。

四种短周期元素W、X、Y、Z,原子序数依次增大,请结合表中信息回答下列问题。
| W | X | Y | Z |
结构或性质 | 最高价氧化物对应的水化物与其气态氢化物反应得到离子化合物 | 焰色反应呈黄色 | 在同周期主族元素形成的简单离子中,离子半径最小 | 最高正价与最低负价之和为零 |
(1)Z在元素周期表中位于 族。
(2)上述元素的最高价氧化物对应的水化物中,有一种物质在一定条件下均能与其他三种物质发生化学反应,该元素是 (填元素符号)。
(3)①下列可作为比较X和Y金属性强弱的依据是 (填序号)。
A.自然界中的含量 B.单质与酸反应时失去的电子数
C.单质与水反应的难易程度 D.最高价氧化物对应水化物的碱性
②从原子结构的角度解释X的金属性强于Y的原因: ,原子半径X>Y,所以原子核对最外层电子的吸引力X<Y,失电子能力X>Y。
(4)W的一种氢化物HW3可用于有机合成,其酸性与醋酸相似。体积和浓度均相等的HW3与X的最高价氧化物对应的水化物的溶液混合,反应的化学方程式是 。
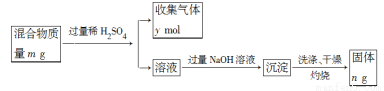
(5)Y单质和Mg组成的混合物是一种焰火原料,某兴趣小组设计如下所示的实验方案,测定混合物中Y的质量分数。能确定混合物中Y的质量分数的数据有 (填序号)。
A.m、n B.m、y C.n、y