题目内容
从石英砂制取并获得高纯硅的主要化学反应如下:
① SiO2+2C![]() Si(粗)+2CO
Si(粗)+2CO
② Si(粗)+2Cl2![]() SiCl4
SiCl4
③ SiCl4+2H2![]() Si(纯)+4HCl
Si(纯)+4HCl
关于上述反应的分析不正确的是
A.①、③是置换反应,②是化合反应
B.高温下,焦炭与氢气的还原性均强于硅
C.任一反应中,每消耗或生成28 g硅,均转移4 mol电子
D.高温下将石英砂、焦炭、氯气、氢气按一定比例混合可得高纯硅
D
解析:
A、B显然正确,C选项由电子守恒可知,28克硅的物质的量为1mol,由+4价化合态转变为单质硅转移电子必为4mol。制取高纯硅是通过连续几步实线的,若将它们混合在一起反应,是无法实现目的的。

练习册系列答案
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案
相关题目
 Si(粗)+2CO
Si(粗)+2CO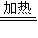 SiCl4
SiCl4 Si(纯)+4HCl
Si(纯)+4HCl