题目内容
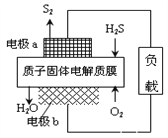
【题目】H2S是一种剧毒气体,对H2S废气资源化利用途径之一是回收能量并得到单质硫,反应原理为:2H2S(g)+O2(g)=S2(s)+2H2O(l) H=-632kJ·mol-1。下图为质子膜H2S燃料电池的示意图。下列说法错误的是( )
A. 电池工作时,电子从电极a经负载流向电极b
B. 实际工作中当反应生成64gS2时,电池内部释放632kJ电能
C. 电极a上发生的电极反应为:2H2S - 4e-=S2 + 4H+
D. 当电路中通过4mol电子时,有4molH+经质子膜进入正极区
【答案】B
【解析】A. 生成S2的电极a是负极,电子从电极a经负载流向电极b,故A正确;B. 实际工作中当反应生成64gS2时,电池外部释放632kJ电能,故B错误;C. 电极a上发生氧化反应,电极反应为:2H2S - 4e-=S2 + 4H+,故C正确D. 当电路中通过4mol电子时,有4molH+经质子膜进入正极区,故D正确。故选B。

练习册系列答案
 优百分课时互动系列答案
优百分课时互动系列答案
相关题目
