题目内容
工业上通过电解饱和的食盐水来制取氯气.现取500 ml含NaCl为11.7 g的饱和食盐水进行电解,
(1)可制得标准状况下Cl2多少升?
(2)所得NaOH的物质的量浓度为多少?(电解前后溶液体积保持不变)
答案:

练习册系列答案
 智趣暑假温故知新系列答案
智趣暑假温故知新系列答案
相关题目
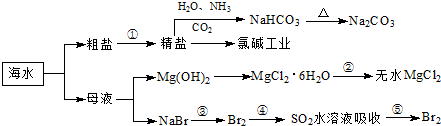
海洋中有丰富的食品、矿产、能源、药物和水产资源,如图为海水利用的部分过程.下列有关说法正确的是( )

| A、在第③、④、⑤步骤中,溴元素均被氧化 | B、制取NaHCO3的原理是利用其在此反应所涉及物质中溶解度最小 | C、用澄清的石灰水可鉴别NaHCO3和Na2CO3 | D、工业上通过电解饱和MgCl2溶液制取金属镁 |
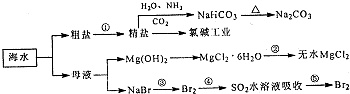
海洋中有丰富的食品、矿产、能源、药物和水产资源,下图为海水利用的部分过程.下列有关说法正确的是
( )
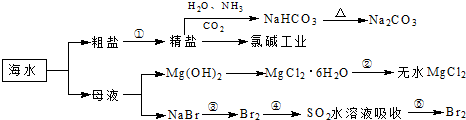
( )

| A、过程①中除去粗盐中的SO42-、Ca2+、Mg2+、Fe3+等杂质,加入的药品顺序为:Na2CO3溶液→NaOH溶液→BaCl2溶液→过滤后加盐酸 | B、用澄清的石灰水可鉴别NaHCO3和Na2CO3 | C、过程②中结晶出的MgCl2?6H2O要在HCl氛围中加热脱水制得无水MgCl2 | D、工业上通过电解饱和MgCl2溶液制取金属镁 |