题目内容
下列关于实验操作能实现目的的是
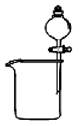 | 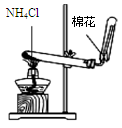 | 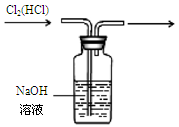 | 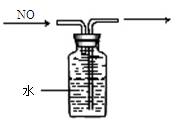 |
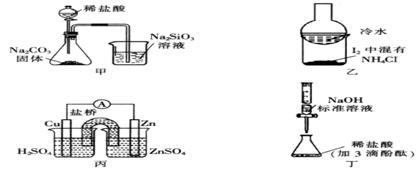
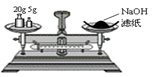
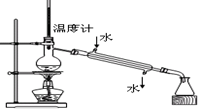
| A.分离碘酒中的碘和酒精 | B.实验室制氨气 | C.除去Cl2中的HCl | D.排水集气法收集NO |
D
试题分析:A、碘在酒精中溶解度很大,很难找到比它溶解度大的,很难分离碘酒中的碘和酒精,故A错误;B、当在试管中加热氯化铵晶体时,氯化铵逐渐受热分解为氯气和氨气,从试管底部消失,但与此同时,在试管上口部位,会出现白色结晶物质,即为受热分解后的氯气和氨气在试管口冷环境下重新化合生成氯化铵,实验室用氯化铵和碱石灰反应制取氨气,即碱与盐反应生成新碱和新盐,故B错误;C、Cl2在NaOH溶液中反应生成Cl-离子和ClO-离子,应用浓硫酸除去,故C错误;D、NO在空气中会与氧气迅速反应生成NO2其密度和空气相差无几,即使可以排空收集,效果也不好,且NO不溶于水,可用排水发收集,故D正确。

练习册系列答案
 精英口算卡系列答案
精英口算卡系列答案 应用题点拨系列答案
应用题点拨系列答案
相关题目
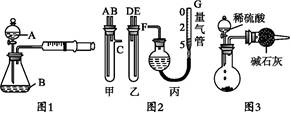
 完成下列填空:
完成下列填空: