题目内容
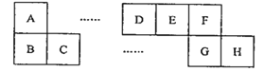
【题目】A~H八种短周期主族元素在周期表中的相对位置如下图所示,已知C元素形成的单质有“国防金属”的美誉,E的最高价氧化物对应的水化物能与E的最简单氢化物反应生成离子化合物。
(1)D元素在周期表中的位置为______。
(2)B、E、F的简单离子半径由大到小的顺序为_____(写离子符号)。
(3)上述元素所形成的气态单质中能用于饮用水消毒的是_____(写化学式)。
(4)B的单质在F的单质中燃烧的火焰颜色为______,所形成化合物的电子式为_____。
(5)C元素的单质可以在D和F组成的一种气态化合物中燃烧,写出该反应的化学方程式____。
【答案】第二周期(或第2周期)第ⅣA族 r(N3-)>r(O2-)>r(Na+)(或N3- >O2->Na+) Cl2或O3 黄色 ![]() 2Mg+CO2
2Mg+CO2![]() 2MgO+C
2MgO+C
【解析】
A~H为八种短周期主族元素,C元素形成的单质有“国防金属”的美誉,则C为Mg元素;E的最高价氧化物对应的水化物能与E的最简单氢化物反应生成离子化合物,则E为N元素,结合元素在周期表的位置可知,A为Li元素,B为Na元素,D为C元素,F为O元素,G为S元素,H为Cl元素,据此解答。
由分析可知:A为Li元素,B为Na元素,C为Mg元素,D为C元素,E为N元素,F为O元素,G为S元素,H为Cl元素。
(1)D为C元素,在周期表中的位置为第二周期第ⅣA族,故答案为:第二周期第ⅣA族。
(2)B为Na元素、E为N元素、F为O元素,B、E、F三种元素的简单离子分别为:Na+、N3-、O2-,电子层结构相同的微粒,核电荷数越大,离子半径越小,所以半径由大到小的顺序为r(N3-)>r(O2-)>r(Na+)(或N3->O2->Na+),故答案为:r(N3-)>r(O2-)>r(Na+)(或N3->O2->Na+)。
(3)上述元素所形成的气态单质中能用于饮用水消毒的是Cl2或O3,故答案为:Cl2或O3。
(4)B的单质在F的单质中燃烧的产物为过氧化钠,火焰颜色为黄色,过氧化钠既含离子键又含共价键,电子式为![]() ,故答案为:黄色;
,故答案为:黄色;![]() 。
。
(5)Mg与二氧化碳反应生成MgO和C,反应方程式为2Mg+CO2![]() 2MgO+C,故答案为:2Mg+CO2
2MgO+C,故答案为:2Mg+CO2![]() 2MgO+C。
2MgO+C。

 金博士一点全通系列答案
金博士一点全通系列答案