题目内容
9.6g元素A与4.2g元素B含有相同的原子数.A、B两原子中,核内质子数与核内中子数相等,已知A元素在其最高价氧化物中的质量分数为40%,在其氢化物中的质量分数为94.21%.试计算:
(1)A、B两元素的相对原子质量.
(2)指出A、B在周期表中的位置.
答案:略
解析:
解析:
|
(1)32 ,14(2)A :第三周期,ⅥA族B:第二周期,ⅤA族设 A的最高价氧化物为 ,则其氧化物为 ,则其氧化物为
则 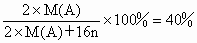
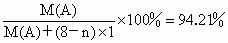
联立解得 M(A)=32故 A的原子核内质子数为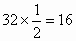 ,A是硫.9.6gA含硫原子0.3mol.则B的相对原子质量为 ,A是硫.9.6gA含硫原子0.3mol.则B的相对原子质量为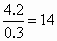 .故B的原子核内质子数为 .故B的原子核内质子数为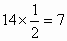 ,B是氮. ,B是氮. |

练习册系列答案
相关题目