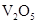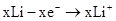题目内容
锂钒氧化物电池的能量密度远远超过其它材料电池,其成本低,便于大量推广,且对环境无污染.电池总反应式为:V2O5+xLi═LixV2O5.下列说法中,不正确的是( )
分析:放电时,该原电池中锂失电子而作负极,V2O5得电子而作正极,负极上发生氧化反应,正极上发生还原反应,阳离子向正极移动.
解答:解:A.该原电池中,锂失电子而作负极,V2O5得电子而作正极,故A错误;
B.向外供电时,该装置是原电池,锂离子向正极移动,故B正确;
C.V2O5得电子而作正极,正极上电极反应式为:V2O5+xe-+xLi+═LixV2O5,故C正确;
D.该原电池中,锂失电子发生氧化反应而作负极,电池反应式为:xLi-xe-═xLi+,故D正确;
故选:A.
B.向外供电时,该装置是原电池,锂离子向正极移动,故B正确;
C.V2O5得电子而作正极,正极上电极反应式为:V2O5+xe-+xLi+═LixV2O5,故C正确;
D.该原电池中,锂失电子发生氧化反应而作负极,电池反应式为:xLi-xe-═xLi+,故D正确;
故选:A.
点评:本题考查原电池原理,明确元素化合价是解本题关键,根据得失电子来分析解答即可,难点是电极反应式的书写.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
锂钒氧化物电池的能量密度远远超过其他材料电池,电池总反应式为:V2O5+xLi→LixV2O5,下列说法不正确的是
| A.向外供电时,锂离子向负极移动 |
| B.负极上反应的物质是锂,正极上反应的物质是V2O5 |
| C.正极的电极反应为:V2O5+xe-+xLi+→LixV2O5 |
| D.负极的电极反应为:xLi-xe-→ xLi+ |
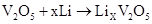 ,下列说法不正确的是
,下列说法不正确的是