题目内容
12.下列实验装置正确且能达到预期实验目的是( )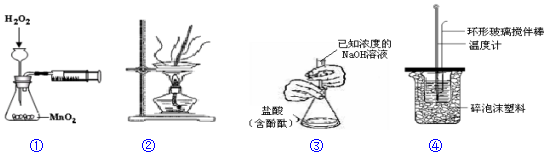
| A. | 装置①用于测定H2O2分解的反应速率 | |
| B. | 装置②用于蒸发FeCl3溶液制取FeC13晶体 | |
| C. | 装置③用于测定未知浓度的盐酸的浓度 | |
| D. | 装置④用于测定中和热 |
分析 A.长颈漏斗不能防止气体逸出;
B.加热时氯化铁易水解生成氢氧化铁;
C.氢氧化钠溶液应放在碱式滴定管中;
D.搅拌、温度的测定及隔热均合理.
解答 解:A.生成的氧气可从长颈漏斗逸出,不能测定气体的体积,应将长颈漏斗改为分液漏斗可实现测定H2O2分解的反应速率,故A错误;
B.加热时氯化铁易水解生成氢氧化铁,应在氯化氢的氛围中加热,以抑制水解,故B错误;
C.氢氧化钠溶液可腐蚀玻璃塞,应放在碱式滴定管中,故C错误;
D.搅拌、温度的测定及隔热均合理,则图中装置用于测定中和热合理,故D正确.
故选D.
点评 本题考查化学实验方案的评价,为高频考点,涉及反应速率测定、盐类水解及中和热测定等,把握物质的性质及实验基本操作为解答的关键,侧重分析与实验能力的考查,题目难度不大.

练习册系列答案
相关题目
2.可以准确判断有机物分子中含有哪些官能团的分析方法是( )
| A. | 核磁共振氢谱 | B. | 质谱 | C. | 紫外光谱 | D. | 红外光谱 |
3.设NA为阿伏加德罗常数的值.下列说法正确的是( )
| A. | 常温常压下,22 g丙烷中含共价键的数目为4NA | |
| B. | 铝热法还原铁的反应中,1 mol Fe3O4被还原成Fe,转移9 mol e- | |
| C. | 标准状况下,16g甲烷分子所含质子数为10NA | |
| D. | 1 mol冰醋酸和足量乙醇在浓硫酸作用下加热反应生成的H2O分子数为NA |
20.与100mL0.1mol/L AlCl3溶液中Cl-的物质的量浓度相等的是( )
| A. | 50mL0.1mol/L NaCl溶液 | B. | 50mL0.15mol/L MgCl2溶液 | ||
| C. | 10mL1.0mol/L FeCl3溶液 | D. | 100mL0.3mol/L KClO3溶液 |
7.胡桐素E的结构简式如图所示.下列说法正确的是( )


| A. | 该分子中有4个手性碳原子 | |
| B. | 该分子中所有碳原子可处于同一平面 | |
| C. | 1mol胡桐素E最多可与3molNaOH反应 | |
| D. | 1mol胡桐素E最多可与4molH2发生加成反应 |
17.化学与生活息息相关,下列说法不正确的是( )
| A. | 用食醋可除去热水壶内壁的水垢 | |
| B. | 工业上电解熔融状态的Al2O3制备Al | |
| C. | 油脂和蛋白质都是高分子化合物 | |
| D. | 利用粮食酿酒经过了淀粉→葡萄糖→乙醇的化学变化过程 |
1.锝(9943Tc )是核医学临床诊断中应用最广的医用核素,其原子核内中子数是( )
| A. | 13 | B. | 43 | C. | 56 | D. | 99 |
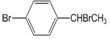 .写出该两步反应所需的试剂及条件:液溴、溴化铁作催化剂,溴、光照
.写出该两步反应所需的试剂及条件:液溴、溴化铁作催化剂,溴、光照 .
.