题目内容
【题目】某化学课外小组查阅资料知:苯和液溴在有铁存在的条件下可反应生成溴苯和溴化氢,此反应为放热反应,他们用右图装 置制取溴苯。先向分液漏斗中加入苯和液溴,再将混合液慢慢滴入反应器A(A下端活塞关闭)中。
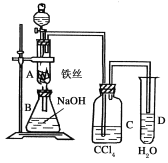
(1)写出A中反应的化学方程式 ___ __________;
(2)实验结束时,打开A下端的活塞,让反应液流入B中,充分振荡, 目的是____ __,写出有关的离子方程式 _______;
(3)C中盛放CCl4的作用是___________ ______;
(4)能证明苯和液溴发生的是取代反应,而不是加成反应,可向试管D中加入AgNO3溶液,若产生淡黄色沉淀,则能证明;另一种验证的方法是向试管D加入____ ____,现象是 ___。
【答案】
(1) ![]() ;
;
(2)使过量的Br2与 NaOH充分反应;2 OH-- + Br2 == Br- + BrO- + H2O ;
(3)除去混在 HBr中的Br2(g);
(4)石蕊试液;溶液变为红色即可证明发生了取代反应。
【解析】
试题分析:(1)在催化剂的作用下,苯环上的氢原子被溴原子所取代,生成溴苯,同时有溴化氢生成,故答案为:![]() ;
;
(2)A中的溴和氢氧化钠反应,可以将溴苯中的溴除去,即Br2+2NaOH=NaBr+NaBrO+H2O,离子方程式为2 OH-- + Br2 == Br- + BrO- + H2O,故答案为:除去溶于溴苯中的溴;2 OH-- + Br2 == Br- + BrO- + H2O;
(3)根据相似相溶原理,溴极易溶于四氯化碳,而溴化氢则不溶,所以C中盛放CCl4的作用是除去溴化氢气体中的溴蒸气,故答案为:除去溴化氢气体中的溴蒸气;
(4)如果发生取代反应,生成溴化氢,溴化氫易溶于水电离出H+和Br-,只要检验含有氢离子或溴离子即可,溴离子的检验:取溶液滴加硝酸银溶液,如果生成淡黄色沉淀就证明是溴离子;氢离子的检验:如果能使紫色石蕊试液变红,就证明含有氢离子,故答案为:石蕊试液;溶液变红色。

 应用题作业本系列答案
应用题作业本系列答案