题目内容
碘是人类必需的生命元素,在人体的生长发育过程中起着重要作用.
(1)人体中碘的重要来源之一是加碘食盐.加碘食盐中的碘元素以碘酸钾(KIO3)的形式存在,其碘元素的化合价是
(2)海带或海苔中含有丰富的碘元素,也是人体碘的一种来源.取海带灰的浸取液加硫酸酸化,再加入少量H2O2溶液与淀粉溶液,溶液变蓝,证明海带中含有碘元素.反应的离子方程式是
(3)2012年3月,北京市最新规定食盐中碘含量标准为(18~33)mg/kg.为测定加碘食盐样品的碘含量,某实验小组设计了如下步骤:
Ⅰ.用天平准确称取10.0g食盐样品,加适量蒸馏水使其完全溶解.
Ⅱ.用稀硫酸酸化所得溶液,加入足量KI溶液,使KIO3与KI反应完全.
Ⅲ.以淀粉为指示剂,逐滴加入物质的量浓度为2.0×10-3mol?L-1的Na2S2O3溶液6.0mL,恰好反应完全.(已知:I2+2S2
=2I-+S4
)
①步骤Ⅱ中反应的离子方程式是
②步骤Ⅲ中判断反应恰好完全的现象是
③上述实验样品中碘含量是
(1)人体中碘的重要来源之一是加碘食盐.加碘食盐中的碘元素以碘酸钾(KIO3)的形式存在,其碘元素的化合价是
+5
+5
.加碘食盐的食用方法是“待食品熟后加入”,说明碘酸钾在受热时易分解
分解
.(2)海带或海苔中含有丰富的碘元素,也是人体碘的一种来源.取海带灰的浸取液加硫酸酸化,再加入少量H2O2溶液与淀粉溶液,溶液变蓝,证明海带中含有碘元素.反应的离子方程式是
H2O2+2I-+2H+=I2+2H2O
H2O2+2I-+2H+=I2+2H2O
.(3)2012年3月,北京市最新规定食盐中碘含量标准为(18~33)mg/kg.为测定加碘食盐样品的碘含量,某实验小组设计了如下步骤:
Ⅰ.用天平准确称取10.0g食盐样品,加适量蒸馏水使其完全溶解.
Ⅱ.用稀硫酸酸化所得溶液,加入足量KI溶液,使KIO3与KI反应完全.
Ⅲ.以淀粉为指示剂,逐滴加入物质的量浓度为2.0×10-3mol?L-1的Na2S2O3溶液6.0mL,恰好反应完全.(已知:I2+2S2
| O | 2- 3 |
| O | 2- 6 |
①步骤Ⅱ中反应的离子方程式是
IO3-+5I-+6H+=3I2+3H2O
IO3-+5I-+6H+=3I2+3H2O
.②步骤Ⅲ中判断反应恰好完全的现象是
蓝色褪去
蓝色褪去
.③上述实验样品中碘含量是
25.4
25.4
mg/kg,符合北京市规定.分析:(1)根据元素化合价的代数和为0判断,结合题意判断碘酸钾的性质;
(2)双氧水具有强氧化性,酸性条件下,双氧水氧化碘离子生成碘单质;
(3)①酸性条件下,碘酸根离子和碘离子发生氧化还原反应生成碘单质;
②碘遇淀粉溶液变蓝色,当完全反应时,溶液褪色;
③根据硫代硫酸钠和碘之间的关系式计算.
(2)双氧水具有强氧化性,酸性条件下,双氧水氧化碘离子生成碘单质;
(3)①酸性条件下,碘酸根离子和碘离子发生氧化还原反应生成碘单质;
②碘遇淀粉溶液变蓝色,当完全反应时,溶液褪色;
③根据硫代硫酸钠和碘之间的关系式计算.
解答:解:(1)根据化合物中各元素的化合价代数和为0知,碘酸钾(KIO3)中碘元素化合价是+5价,根据题意知,
碘酸钾在受热时易分解,故答案为:+5,分解;
(2)双氧水具有强氧化性,酸性条件下,双氧水氧化碘离子生成碘单质,自身被还原生成水,反应方程式为:H2O2+2I-+2H+=I2+2H2O,故答案为:H2O2+2I-+2H+=I2+2H2O;
(3)①酸性条件下,碘酸根离子和碘离子发生氧化还原反应生成碘单质,离子反应方程式为:
IO3-+5I-+6H+=3I2+3H2O,
故答案为:IO3-+5I-+6H+=3I2+3H2O;
②碘遇淀粉试液变蓝色,如果溶液中不存在碘单质,则溶液蓝色褪去,故答案为:蓝色褪去;
③IO3-+5I-+6H+=3I2+3H2O㈠、I2+2 S2O32-=2I-+S4O62-㈡,将方程式㈠+㈡×3得IO3-+6H++6S2O32-=3H2O+I-+3S4O62-,设碘酸钾中碘的质量是x,
IO3-+6H++6S2O32-=3H2O+I-+3S4O62-,
127g 6mol
x 2.0×10-3 mol?L-1×0.006L
x=
=0.254mg,每10g食盐中含有0.254mg碘,则每1Kg食盐中含有碘25.4mg,所以符合规定,故答案为:25.4.
碘酸钾在受热时易分解,故答案为:+5,分解;
(2)双氧水具有强氧化性,酸性条件下,双氧水氧化碘离子生成碘单质,自身被还原生成水,反应方程式为:H2O2+2I-+2H+=I2+2H2O,故答案为:H2O2+2I-+2H+=I2+2H2O;
(3)①酸性条件下,碘酸根离子和碘离子发生氧化还原反应生成碘单质,离子反应方程式为:
IO3-+5I-+6H+=3I2+3H2O,
故答案为:IO3-+5I-+6H+=3I2+3H2O;
②碘遇淀粉试液变蓝色,如果溶液中不存在碘单质,则溶液蓝色褪去,故答案为:蓝色褪去;
③IO3-+5I-+6H+=3I2+3H2O㈠、I2+2 S2O32-=2I-+S4O62-㈡,将方程式㈠+㈡×3得IO3-+6H++6S2O32-=3H2O+I-+3S4O62-,设碘酸钾中碘的质量是x,
IO3-+6H++6S2O32-=3H2O+I-+3S4O62-,
127g 6mol
x 2.0×10-3 mol?L-1×0.006L
x=
| 2.0×10-3 mol?L-1×0.006L×127g |
| 6mol |
点评:本题考查了氧化还原反应、碘的检测等知识点,难点是计算食盐中碘含量,明确碘酸钾和硫代硫酸钠的关系式是解本题关键,难度中等.

练习册系列答案
相关题目
 )
) )
) 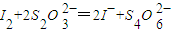 )
)