题目内容
13.某一反应2A+B═2C,开始时A的浓度4mol/L,2min后测得A的浓度为3mol/L,请分别用A、B、C的浓度变化来表示该反应的速率,v( A)=0.5mol/(L•min) v(B)=0.25mol/(L•min) v( C)=0.5mol/(L•min).分析 根据A的浓度的改变量表示出v( A)=$\frac{△C(A)}{△t}$,然后根据反应速率之比等于计量数之比计算出B和C的反应速率.
解答 解:开始时A的浓度4mol/L,2min后测得A的浓度为3mol/L,故A的浓度的该变量△c(A)=1mol/L,故v( A)=$\frac{△C(A)}{△t}$=$\frac{1mol/L}{2min}$=0.5mol/(L•min);
而在反应中,反应速率之比等于计量数之比,故v( B)=v( A)×$\frac{1}{2}$=0.25mol/(L•min);
v( C)=v( A)=0.5mol/(L•min);
故答案为:0.5mol/(L•min);0.25mol/(L•min);0.5mol/(L•min).
点评 本题考查化学反应速率的计算,难度不大,注意反应速率的理解,通常有定义法与化学计量数法两种计算方法.

练习册系列答案
 53随堂测系列答案
53随堂测系列答案
相关题目
4.下表是某地区市场上销售的一种“加碘食盐”包装袋上的部分文字说明.请根据此表,结合化学和生物学科的知识,回答下列问题.
(1)要在食盐中加碘,是因为碘是人体内合成甲状腺激素的主要原料,缺碘会引起疾病.
(2)食盐中加碘,这碘指的是元素(填“单质”、“化合物”或“元素”),其中碘元素的化合价为+5.
(3)根据含碘盐的食用方法可推测碘元素的化学性质,碘酸钾在受热时容易分解.
| 配料表 | 精制海盐、碘酸钾 |
| 含碘量 | 20~40mg/kg |
| 卫生许可证号 | ××卫碘字(1999)第001号 |
| 分装日期 | 见封底 |
| 储藏方法 | 密封、避光、防潮 |
| 食用方法 | 烹调时,待食品熟后加入碘盐 |
(2)食盐中加碘,这碘指的是元素(填“单质”、“化合物”或“元素”),其中碘元素的化合价为+5.
(3)根据含碘盐的食用方法可推测碘元素的化学性质,碘酸钾在受热时容易分解.
8.根据有机化合物的命名原则,下列命名正确的是( )
| A. | 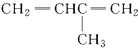 3-甲基-1,3-丁二烯 3-甲基-1,3-丁二烯 | B. |  2-羟基丁烷 2-羟基丁烷 | ||
| C. | CH3CH(C2H5)CH2CH2CH3 2-乙基戊烷 | D. | CH3CH(CH3)CH2COOH 3-甲基丁酸 |
3.在2A(g)+B(g)?3C(g)+4D(g)反应中,表示该反应速率最快的是( )
| A. | v(A)=0.6 mol/(L•s) | B. | v (B)=0.4mol/(L•s) | C. | v (C)=0.9 mol/(L•s) | D. | v (D)=1 mol/(L•s) |
 ,D原子的原子结构示意图为
,D原子的原子结构示意图为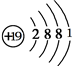 ,C+离子的结构示意图为
,C+离子的结构示意图为 .
. (1)意大利科学家FulvioCacace等获得了极具理论研究意义的N4分子.N4分子结构如图所示.已知断裂1mol N-N吸收167kJ热量,生成1mol N≡N放出942kJ.根据以上信息和数据,计算1molN4气体转变为N2气体的△H=-882 kJ•mol-1
(1)意大利科学家FulvioCacace等获得了极具理论研究意义的N4分子.N4分子结构如图所示.已知断裂1mol N-N吸收167kJ热量,生成1mol N≡N放出942kJ.根据以上信息和数据,计算1molN4气体转变为N2气体的△H=-882 kJ•mol-1