题目内容
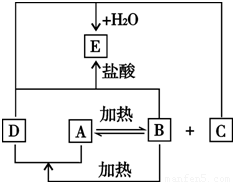
已知A、B、D、E中有一种元素相同,这些物质化学式中只含有这种元素的一
个原子,且E在C中可燃烧,火焰呈蓝紫色,A、B、D是白色固体,E是浅黄色固体,A、B、
D、E均不含结晶水,A、B、D其焰色反应呈黄色.
(1)写出下列物质的化学式:
A______ B______D______ E______
(2)写出下列反应方程式(是离反应的写出离子方程式)
①C+D+H2O→E______②B+D+HCl→E______
(3)有一位同学把B放在封闭的容器中加热至恒重,试问恒重的固体物可能含有哪些物质?(可不写满或增加)
①______;②______;③______.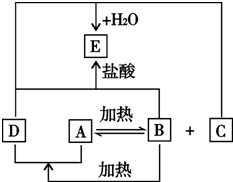
个原子,且E在C中可燃烧,火焰呈蓝紫色,A、B、D是白色固体,E是浅黄色固体,A、B、
D、E均不含结晶水,A、B、D其焰色反应呈黄色.
(1)写出下列物质的化学式:
A______ B______D______ E______
(2)写出下列反应方程式(是离反应的写出离子方程式)
①C+D+H2O→E______②B+D+HCl→E______
(3)有一位同学把B放在封闭的容器中加热至恒重,试问恒重的固体物可能含有哪些物质?(可不写满或增加)
①______;②______;③______.

依据转化关系和反应条件,E在C中可燃烧,E是浅黄色固体,火焰呈蓝紫色推断E为S,C为O2,已知A、B、D、E中有一种元素相同,这些物质化学式中只含有这种元素的一个原子,且A、B、D是白色固体,A、B、D、E均不含结晶水,A、B、D其焰色反应呈黄色证明含有钠元素;说明ABD为含钠元素和硫元素的化合物,依据转化关系结合硫及其化合物的性质可知,C(O2)+D+H2O=E(S),结合所含有的元素推断D为Na2S,转化关系中D(Na2S)+B+HCl=E(S),说明B为Na2SO3;依据B(Na2SO3)=A+D(Na2S),化合价从+4价变化为-2价,另一种元素化合价一定升高为+6价,结合组成元素判断A为Na2SO4;
(1)根据推断可知,A的化学式为Na2SO4,B的化学式为Na2SO3,D的化学式为Na2S,E的化学式为S,故答案为:Na2SO4;Na2SO3;Na2S;S;
(2)①C(O2)+D(Na2S)+H2O→E是离反应,反应离子方程式为2S2-+O2+2H2O=2S+4OH-;,故答案为:2S2-+O2+2H2O=2S+4OH-;
②B(Na2SO3)+D(Na2S)+HCl→E(S),反应是离子反应,反应的离子方程式为SO32-+2S2-+6H+=3S+3H2O,故答案为:SO32-+2S2-+6H+=3S+3H2O;
(3)把B(Na2SO3)放在封闭的容器中加热至恒重,恒重的固体物可能含有的物质为:①弱密闭容器中无氧气则可能为Na2SO3;②弱密闭容器中有氧气,可能含有Na2SO4、Na2S;③若密闭容器中亚硫酸钠部分氧化分解,则可能含有Na2SO4、Na2S、Na2SO3,
故答案为:Na2SO3;Na2SO4、Na2S;Na2SO4、Na2S、Na2SO3.
(1)根据推断可知,A的化学式为Na2SO4,B的化学式为Na2SO3,D的化学式为Na2S,E的化学式为S,故答案为:Na2SO4;Na2SO3;Na2S;S;
(2)①C(O2)+D(Na2S)+H2O→E是离反应,反应离子方程式为2S2-+O2+2H2O=2S+4OH-;,故答案为:2S2-+O2+2H2O=2S+4OH-;
②B(Na2SO3)+D(Na2S)+HCl→E(S),反应是离子反应,反应的离子方程式为SO32-+2S2-+6H+=3S+3H2O,故答案为:SO32-+2S2-+6H+=3S+3H2O;
(3)把B(Na2SO3)放在封闭的容器中加热至恒重,恒重的固体物可能含有的物质为:①弱密闭容器中无氧气则可能为Na2SO3;②弱密闭容器中有氧气,可能含有Na2SO4、Na2S;③若密闭容器中亚硫酸钠部分氧化分解,则可能含有Na2SO4、Na2S、Na2SO3,
故答案为:Na2SO3;Na2SO4、Na2S;Na2SO4、Na2S、Na2SO3.

练习册系列答案
 一线名师提优试卷系列答案
一线名师提优试卷系列答案
相关题目
 (2011?宝鸡模拟)已知A、B、D、E中有一种元素相同,这些物质化学式中只含有这种元素的一
(2011?宝鸡模拟)已知A、B、D、E中有一种元素相同,这些物质化学式中只含有这种元素的一
 已知A、B、D、E中有一种元素相同,这些物质化学式中只含有这种元素的一
已知A、B、D、E中有一种元素相同,这些物质化学式中只含有这种元素的一