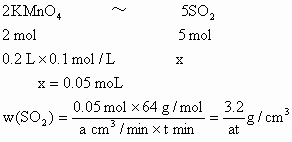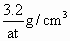题目内容
中央电视台每晚《晚间新闻》后,都要预报42个重点城市的空气质量,它一般将这些城市空气中的 和可吸入颗粒的含量(可用
和可吸入颗粒的含量(可用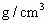 )分为8个等级.目前,测定空气中
)分为8个等级.目前,测定空气中 含量主要用氧化还原反应原理测定.假如给你一个气体流速管(单位时间内通过气体的体积恒定,且无除尘和吸收气体作用),请你设计一个实验装置,测定你所在地区的空气中
含量主要用氧化还原反应原理测定.假如给你一个气体流速管(单位时间内通过气体的体积恒定,且无除尘和吸收气体作用),请你设计一个实验装置,测定你所在地区的空气中 和可吸入颗粒的含量.
和可吸入颗粒的含量.
已知: 气体与酸性
气体与酸性 溶液反应时,
溶液反应时, 被还原为
被还原为 ,
, 被氧化成
被氧化成 .
.
现有药品:0.1mol/L的酸性 溶液、颗粒吸附剂、品红试液、pH试纸.
溶液、颗粒吸附剂、品红试液、pH试纸.
现有仪器:密闭容器用 或
或 表示,敞口仪器用
表示,敞口仪器用 ;导管用
;导管用 ;气体流速管用
;气体流速管用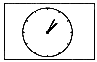 .
.
(1)配制200mL0.1mol/L酸性 溶液,需用仪器有玻璃棒、____________、________________、___________、_______________.玻璃棒的作用是____________________、__________________________.
溶液,需用仪器有玻璃棒、____________、________________、___________、_______________.玻璃棒的作用是____________________、__________________________.
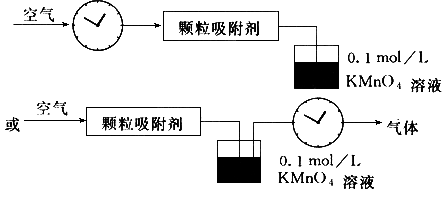
(2)画出测定空气中 和可吸入颗粒含量的实验装置图(并指出仪器中的药品).
和可吸入颗粒含量的实验装置图(并指出仪器中的药品).
(3)若气体流速管中气体流速为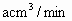 ,当tmin后200mL0.1mol/L
,当tmin后200mL0.1mol/L 溶液恰好褪色.求空气中
溶液恰好褪色.求空气中 的含量(
的含量(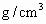 ).
).
(4)若要测定空气中可吸入颗粒的含量,需要测出的数据有___________.
空气中 的含量还可用检测管测定,其原因是:指示剂
的含量还可用检测管测定,其原因是:指示剂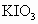 发生作用,可能发生的反应(未配平)有:
发生作用,可能发生的反应(未配平)有:
①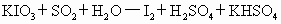
②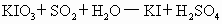
(5)检气管是按照上述两个方程式中的____________方程式设计的.如果是按另一方程式设计的实验程序,能检测出空气中的二氧化硫的含量吗?__________________(填“能”“不能”或“无法确定”),理由是_____________________________________________________________.
(6)为了能够准确地测定出空气中的二氧化硫的含量,拉动采样器的手柄则应该注意的是____________________,理由是____________________.
解析:
|
解析: (1)配制一定物质的量浓度的溶液所用仪器:容量瓶、胶头滴管、烧杯、玻璃棒、托盘天平.(2) 玻璃棒在溶解时作用为搅拌,转移溶液时作用为引流.(3) 由关系式:
(4) 测气体前后的质量差.(5) 反应①产生单质碘使溶液有颜色,反应②溶液颜色无变化.答案: (1)容量瓶 胶头滴管 烧杯 托盘天平 搅拌 引流(2) 见图
(3) (4) 吸收前和吸收后颗粒吸附剂和盛放仪器的质量(5) ① 不能 反应②溶液颜色没有变化(6) 慢慢拉动,既不能太快,也不能太慢 为避免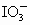 被还原成 被还原成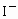 或 或 不易被氧化 不易被氧化 |