题目内容
下图![]() 为直流电源,
为直流电源,![]() 为浸透饱和氯化钠溶液和酚酞试液的滤纸,
为浸透饱和氯化钠溶液和酚酞试液的滤纸,![]() 为电镀槽。接通电路后,发现c点显红色,请填空:
为电镀槽。接通电路后,发现c点显红色,请填空:
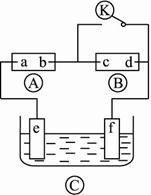
?
(1)电源A上的a为_______ 极。?
(2)滤纸B上发生的总化学反应方程式为__________________。?
(3)欲在电镀槽中实现铁上镀锌,接通K点,使c、d两点短路,则电极e上发生的反应为________。电极f上发生的反应为______,槽中盛放的电解液可以是______或______ (只要求填写两种电解质溶液)。?
(1)正?
![]() ?
?
(3)Zn-2e-![]() Zn2+ Zn2++2e-
Zn2+ Zn2++2e-![]() Zn ZnSO4溶液 ZnCl2溶液
Zn ZnSO4溶液 ZnCl2溶液
解析:
接通电路后c点显红色,说明在c点发生了2H2O+2e-![]() H2↑+2OH-反应,即c点是电解池的阴极,电源?的b极为负极,a极为正极,滤纸上发生的是电解饱和食盐水的反应;在电镀时,与电源正极a相连的e极为阳极,应接锌板,而与电源负极b相连的f极为阴极,应接镀锌制件,电极反应分别为:阳(e)极Zn-2e-
H2↑+2OH-反应,即c点是电解池的阴极,电源?的b极为负极,a极为正极,滤纸上发生的是电解饱和食盐水的反应;在电镀时,与电源正极a相连的e极为阳极,应接锌板,而与电源负极b相连的f极为阴极,应接镀锌制件,电极反应分别为:阳(e)极Zn-2e-![]() Zn2+;阴(f)极Zn2++2e-
Zn2+;阴(f)极Zn2++2e-![]() Zn,电解槽中应盛含有Zn2+的溶液。?
Zn,电解槽中应盛含有Zn2+的溶液。?

(9分)某种碳酸锰矿的主要成分有MnCO3、MnO2、FeCO3、MgO、SiO2、Al2O3等。已知碳酸锰难溶于水。一种运用阴离子膜电解法的新技术可用于从碳酸锰矿中提取金属锰,流程如下:

阴离子膜法电解装置如下图所示:

(1)写出用稀硫酸溶解碳酸锰反应的离子方程式: 。
(2)已知Ksp
(Fe(OH)3) = 4 ´10–38,假设溶液中Fe3+离子浓度为0.1 mol·L–1,则开始生成Fe(OH)3
沉淀的pH是_________,沉淀完全的pH是_________。(可能用到的数据:lg =
-0.1 lg
=
-0.1 lg =0.2)
=0.2)
(3)已知不同金属离子生成氢氧化物沉淀所需的pH如下表:
|
离子 |
Fe3+ |
A13+ |
Fe2+ |
Mn2+ |
Mg2+ |
|
开始沉淀的pH |
1.2 |
3.7 |
7.0 |
7.8 |
9.3 |
|
沉淀完全的pH |
3.7 |
4.7 |
9.6 |
9.8 |
10.8 |
加氨水调节溶液的pH等于6,则“滤渣(待处理)”的成分是 (写化学式),滤液中含有的阳离子有H+和 (写符号)。
(4)在浸出液里锰元素只以Mn2+的形式存在,且滤渣A中也无MnO2,请用离子方程式解释原因: 。
(5)电解装置中箭头表示溶液中阴离子移动的方向,则A电极是直流电源的 极。实际生产中,阳极以稀硫酸为电解液,阳极的电极反应式为 。
(6)该工艺之所以采用阴离子交换膜,是为了防止Mn2+进入阳极区发生副反应生成MnO2造成资源浪费,写出该副反应的电极反应式: 。




