题目内容
下列离子在溶液中因发生氧化还原反应而不能大量共存的是
- A.H3O+、NO3-、Fe2+、Na+
- B.Ag+、NO3-、Cl-、K+、
- C.K+、Ba2+、OH-、SO42-
- D.Cu2+、NH4+、Br-、OH-
A
分析:注意题目要求,离子反应的类型是氧化还原反应,离子组中应具有较强氧化性和还原性的离子,并能发生反应.
解答:A、Fe2+离子具有还原性,NO3-离子在酸性条件下具有强氧化性,二者发生氧化还原反应而不能大量共存,故A选;
B、Ag+与Cl-离子因生成沉淀而不能共存,但发生的不是氧化还原反应,不符合题目要求,故B不选;
C、Ba2+与SO42-离子因生成沉淀而不能共存,但发生的不是氧化还原反应,不符合题目要求,故C不选;
D、Cu2+与OH-离子因生成沉淀而不能共存,NH4+与OH-离子生成NH3?H2O而不能大量共存,但发生的不是氧化还原反应,不符合题目要求,故D不选.
故选A.
点评:本题考查离子共存问题,题目难度不大,注意题目要求为解答本题的关键.
分析:注意题目要求,离子反应的类型是氧化还原反应,离子组中应具有较强氧化性和还原性的离子,并能发生反应.
解答:A、Fe2+离子具有还原性,NO3-离子在酸性条件下具有强氧化性,二者发生氧化还原反应而不能大量共存,故A选;
B、Ag+与Cl-离子因生成沉淀而不能共存,但发生的不是氧化还原反应,不符合题目要求,故B不选;
C、Ba2+与SO42-离子因生成沉淀而不能共存,但发生的不是氧化还原反应,不符合题目要求,故C不选;
D、Cu2+与OH-离子因生成沉淀而不能共存,NH4+与OH-离子生成NH3?H2O而不能大量共存,但发生的不是氧化还原反应,不符合题目要求,故D不选.
故选A.
点评:本题考查离子共存问题,题目难度不大,注意题目要求为解答本题的关键.

练习册系列答案
相关题目
(14分)
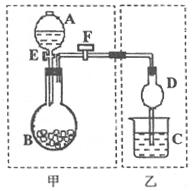
I(8分)用如图所示装置进行实验,将A中液体加入到B中,在甲装置内制备某种气体,在乙装置对甲中产生的气体进行性质实验。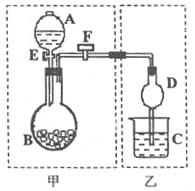
(1)若要检查甲装置的气密性,具体的操作步骤为 。
(2)若在分液漏斗A中盛浓盐酸:
①若B中盛有某种紫黑色固体,C中盛有KI淀粉溶液,旋开F.E后,C中的溶液变蓝色,则B中固体为 ;继续通气体于C中,足够长的时间后,发现C中溶液蓝色褪去,这是因为在溶液中的I2被氧化为HIO3,写出此反应的化学方程式 。
②若B中盛有某种无色液体,当C中盛石蕊试液时,旋开F.E后,C中的溶液变红色,当C中盛品红溶液时,旋开F.E后,品红溶液不褪色,则B中无色液体为 。
当C中盛 溶液时,写出C中反应的化学方程式 。但我们发现在将A中液体加入圆底烧瓶中速度过快会有危险,你认为应如何简单的改进该装置就能避免该危险: 。
溶液时,写出C中反应的化学方程式 。但我们发现在将A中液体加入圆底烧瓶中速度过快会有危险,你认为应如何简单的改进该装置就能避免该危险: 。
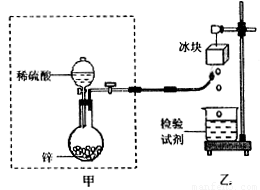
Ⅱ(6分)氢气在空气中燃烧生成水:但有的同学会提出:氢气在空气中燃烧会不会生成H2O2;根据我们的经验,H2O2不稳定,即便是有少量H2O2生成,也会因火焰的高温而分解。某课外兴趣小组利用上题中的甲装置设计了如下图所示装置验证H2在空气中燃烧的产物中是否含有H2O2。试填空:
(1)甲同学从下列试剂中选择了一种检验试剂,成功检测到了H2O2的存在,该试剂是
| A.淀粉溶液 | B.氯化钠溶液 |
| C.氢氧化钠溶液 | D.淀粉碘化钾酸性溶液 |
反应的离子方程式为 。
(2)乙同学用较稀的酸性高锰酸钾溶液作为检验试剂,实验时观察到高锰酸钾溶液褪色(生成Mn2+),由此也证明了氢气燃烧有H2O2,写出该反应的离子方程式:
。
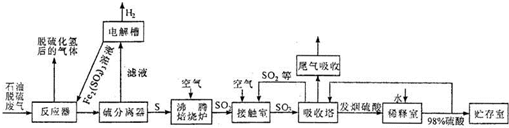

 溶液时,写出C中反应的化学方程式
。但我们发现在将A中液体加入圆底烧瓶中速度过快会有危险,你认为应如何简单的改进该装置就能避免该危险:
。
溶液时,写出C中反应的化学方程式
。但我们发现在将A中液体加入圆底烧瓶中速度过快会有危险,你认为应如何简单的改进该装置就能避免该危险:
。