题目内容
在密闭容器中,反应X2(g)+2Y2(g)? ?2X Y2(g) ΔH<0达到甲平衡,若只改变某一条件再达到乙平衡,则对此过程条件改变的分析正确的是
?2X Y2(g) ΔH<0达到甲平衡,若只改变某一条件再达到乙平衡,则对此过程条件改变的分析正确的是
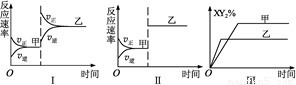
A.图Ⅰ由甲至乙加入适当催化剂 B.图Ⅱ由甲至乙扩大容器体积
C.图Ⅲ由甲至乙增大压强 D.图Ⅲ由甲至乙升高温度
【答案】
D
【解析】
试题分析:A项:催化剂不能使化学平衡移动,故错;B项:化学平衡没移动,应该加入的是催化剂,故错;C项:增大压强,平衡正向移动,故错。故选D。
考点:化学平衡的移动
点评:本题考查温度温度、压强和催化剂对平衡移动的影响,题目难度中等,注意分析表中数据以及图象的曲线的变化,学习中注意加强该方面能力的培养。

练习册系列答案
相关题目
在密闭容器中发生反应:aX(g)+bY(g)?cZ(g)+dW(g),反应达到平衡后,保持温度不变,将气体体积压缩到原来的一半,当再次达到平衡时,W的浓度为原平衡的1.8倍.下列叙述中不正确的是( )